
25.(10分)有下列溶液:A、氢氧化钠溶液;B、氢氧化钡溶液;C、硫酸铝溶液;D、明矾溶液;E、混有少量硝酸的硫酸镁溶液;F、氯化铁溶液;任取其中的一种溶液(甲)逐滴加入到另一种溶液(乙)中至过量,观察到自始至终均有白色沉淀。试回答下列问题:
(1)产生上述实验现象的试剂组合有(请用字母代号逐一列出,表格各栏可填满,可不填满,也可补充)
|
组别 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
甲 |
B |
|
|
|
|
|
|
|
|
乙 |
D |
|
|
|
|
|
|
|
(2)请在图a的坐标中作出第1组实验所得沉淀的物质的量(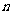 沉淀/mol)随B溶液体积(VB/L)变化的曲线。
沉淀/mol)随B溶液体积(VB/L)变化的曲线。

(3)图b是某一组实验中所得沉淀的物质的量(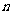 沉淀/mol)随甲溶液中溶质的物质的量(n甲/mol)变化的曲线。符合下图曲线的试剂组合是:甲 (填化学式)、乙 (填化学式)。
沉淀/mol)随甲溶液中溶质的物质的量(n甲/mol)变化的曲线。符合下图曲线的试剂组合是:甲 (填化学式)、乙 (填化学式)。
①若实验时取用的乙溶液为500 mL,试计算乙溶液中溶质的物质的量的浓度。
②若向500 mL乙溶液中滴加1000 mL甲溶液时恰好得到6 mol(1<b<5)白色沉淀,请计算甲溶液中溶质的物质的量浓度。
24.(8分)治理硝酸工业尾气中的氮氧化物(NO、NO2)的化学原理为:2NO2+2NaOH
==NaNO3+NaNO2+H2O; NO2+NO+2NaOH==2NaNO2+H2O。现有标准状况下的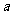 L NO2(其中N2O4的体积分数为20%)、
L NO2(其中N2O4的体积分数为20%)、 L NO的混合气体,恰好被200mL一定浓度的NaOH溶液完全吸收。
L NO的混合气体,恰好被200mL一定浓度的NaOH溶液完全吸收。
(1)根据上述条件可知, 的值应在 范围中;
的值应在 范围中;
(2)设生成的NANO3的物质的量为 ,NaNO2的物质的量为
,NaNO2的物质的量为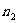 。
。
①当产物全部为NaNO3时,求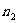 的值;
的值;
②当产物中兼有NANO3和NaNO2时,求 和
和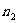 的值;
的值;
③求上述NaOH溶液的物质的量浓度。
23.(10分)烯烃被酸性KMnO4氧化的产物与不饱和碳原子上的氢原子数有关,如:

具有结构 的有机物称之为酮,能发生如下反应:
的有机物称之为酮,能发生如下反应:

从有机物A出发,经过图所示一系列反应可以合成天然橡胶F。(反应条件未注明)

A分子中所有C原子有可能都在同一平面上,其一氯取代物只有两种同分异构体;天然橡胶F的结构为: 。
。
请按要求填空:
(1)A的结构简式是 ,C的结构简式是 ;
(2)指出下列反应的类型:反应③ ,反应⑤ ;
(3)写出下列反应的化学方程式:
反应② ,
反应⑥ 。
22.(8分)相对分子质量为94.5的有机物A,在一定条件下可以发生如图所示的转化(其他产物和水已略去)。
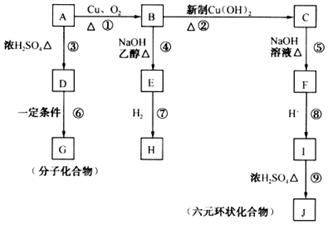
请回答下列问题:
(1)写出下列物质的结构简式:A ,J 。
(2)上述①-⑨的反应中, 是消去反应(填编号)。
(3)写出B→C的化学反应方程式: 。
(4)有机物I在一定条件下可合成一种环保高分子材料,则该高分子结构简式为
。
(三)检测:取10mL水样倒入比色管中,加少许对氨基苯磺酸,显色后与标准色阶对比。
请填写以下空白:
a.比色法的基本依据是 ;
b.若水样显色后与色阶中的5号颜色相同.则表明水样中NO 含量为 mg/L。
含量为 mg/L。
c.用NANO2直接配制溶液B的缺点是 。
d.如果水样显色后比6号还深。应采取的措施是 。
(3)COD的测定目前通常采用高锰酸钾溶液法,废水中多数有机物都可以被氧化,但反应过程相当复杂,一般用C表示有机物。
①请写出水体中有机物在酸|生条件下被高锰酸钾溶液氧化的离子方程式
;
②你建议使用 (选填“稀硫酸”“稀硝酸”“稀盐酸”)酸化废水水样,理由是 。
(4)为检测工业废水中苯酚的含量,需进行下列实验:
①配制标准溴试剂并测定其浓度。将KBrO3与过量KBr混合溶于水配成标准溴试剂。取标准溴试剂25.00mL,依次加入过量稀硫酸和过量KI溶液,然后用0.1000mol/L的Na2S2O3溶液滴定,反应为I2+2S2O ==2I
==2I +S4O
+S4O ,结果消耗18.75mL Na2S2O3溶液。写出标准溴试剂加入稀硫酸产生单质溴的化学方程式,并汁算标准溴试剂中KBrO3的物质的量浓度。
,结果消耗18.75mL Na2S2O3溶液。写出标准溴试剂加入稀硫酸产生单质溴的化学方程式,并汁算标准溴试剂中KBrO3的物质的量浓度。
②测定工业废水中苯酚的含量。取工业废水100.00mL与25.00mL上述标准溴试剂混合,再加入过量稀硫酸,充分反应后又加入过量KI。用0.1000mol/L的Na2S2O3溶液滴定,结果消耗Na2S2O3溶液14.25mL。求工业废水中苯酚的含量(用mg/L表示)。
(二)配制标准色阶:取6只规格为10mL的比色管(即质地、大小、厚薄相同且有塞的平底试管),分别加入体积不等的溶液B,并稀释至10mL,再加入少许(约0.3g)对氨基苯磺酸粉末,实验结果如下表所示:
|
色阶序号 |
l |
2 |
3 |
4 |
5 |
6 |
|
加入溶液B的体积/mL |
0 |
2.0 |
4.0 |
6.0 |
8.0 |
10.0 |
|
反应后溶液颜色 |
由无色变为由浅到深的樱桃红色 |
(一)配制标准溶液:称取0.30g NaNO2,溶于水后在容量瓶中稀释至1L得溶液A,移取5mL溶液A,稀释至1L,得溶液B。
21.(10分)COD(废水的化学耗氧量)是在一定条件下,采用一定的强氧化剂处理水样时。所消耗的氧化剂的量再转化为用氧气作氧化剂时消耗的氧气的量.单位mg/L,它是表示水中还原性物质多少的一个指标。《2004年江苏省环境公报》指出:2004年全省废水排放总量为46.6亿t,其中工业废水排放量为26.3亿t,生活污水排放量为20.3亿t。废水中COD排放总量为85.4万t,其中工业废水中COD排放量为29.8万t,占COD排放总量的34.9%;生活污水中COD排放量为55.6万t,占COD排放总量的65.1%。氨氮排放总量为7.3万t,石油类排放总量为1804.3t,挥发酚排放总量为74.3t。回答下列问题:
(1)江苏省水污染的特征是 。
(2)某校研究性学习小组拟选择“本地水污染情况分析”的课题进行探究。
①如果你参加该课题的探究,你的子课题是 ,选择该子课题的理由是 。
②水中的NO 是含氮有机物分解的产物,其浓度的大小是水源污染的标志之一。检测水中的NO
是含氮有机物分解的产物,其浓度的大小是水源污染的标志之一。检测水中的NO 可用比色法,其步骤是:
可用比色法,其步骤是:
20.(10分)A-N均为中学化学中的常见物质,其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料,单质M是目前使用量最大的金属,常温下B、E、F为气体,G为无色液体,这些物质在一定条件下存在如图所示转化关系,其中有些反应物或生成物已经略去。回答下列问题:

(1)H的化学式为 ,D的电子式为 。
(2)B和N的离子反应方程式为 。
(3)D与G反应的离子方程式为 。
(4)G与M反应的化学方程式为 。
(5)I可用于净化水,其原因是 。
19.(8分)请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有 种。
(27第ⅢA、VA族元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。GA原子的电子排布式为 。在GaN晶体中,每个Ga原子与 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为 。在四大晶体类型中,GaN属于 晶体。
(3)在极性分子NCl3中,N原子的化合价为一3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是 (填化学式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com