
10.1 g H2完全燃烧生成液态水放出142.9 kJ热量,表示该反应的热化学方程式正确的是
( )
A.2H2 + O2 == 2H2O ΔH=-571.6kJ·mol-1
B.H2(g)+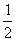 O2(g)== H2O( l ) ΔH=-142.9
kJ·mol-1
O2(g)== H2O( l ) ΔH=-142.9
kJ·mol-1
C.H2(g)+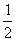 O2(g)== H2O
( l ) ΔH=-285.8
kJ·mol-1
O2(g)== H2O
( l ) ΔH=-285.8
kJ·mol-1
D.2H2(g)+O2(g)== 2H2O ( g ) ΔH=-571.6 kJ·mol-1
9.下列变化一定不可逆的是
A.溶解 B.水解 C.电解 D.电离
8.把下列溶液蒸干灼烧最后得到的固体产物仍是原来溶液中的溶质的是 ( )
A.FeCl3 B.NaHCO3 C.AlCl3 D.K2CO3
7.下列方程式书写正确的是 ( )
A.NaHCO3在水溶液中的电离方程式:NaHCO3  Na++HCO3-
Na++HCO3-
B.H2SO3的电离方程式H2SO3  2H++SO32-
2H++SO32-
C.CO32-的水解方程式:CO32-+2H2O
 H2CO3+2OH-
H2CO3+2OH-
D.HS-的水解方程式:HS-+H2O
 H2S+OH-
H2S+OH-
6.将0.01mol/L的盐酸加水稀释10倍后溶液的pH值是 ( )
A.2 B.11 C.0.01 D.3
5.2A(g)+B(g) 3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
A.v(A)=0.7 mol·L-1·min-1 B.v(B)=0.3 mol·L-1·min-1
C.v(C)=0.9 mol·L-1·min-1 D.v(D)=1.1 mol·L-1·min-1
4.用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是 ( )
A.稀HCl溶液 B.稀Na2SO4溶液
C.CuCl2溶液 D.酸性AgNO3溶液
3.常温下,下列变化过程不是自发的是 ( )
A.石灰石的分解 B.原电池产生电流
C.在密闭条件下体系从有序变为无序 D.铁在潮湿空气中生锈
2.下列溶液一定呈中性的是
A.pH=7的溶液
B.c(H+)=1.0×10-7 mol/L的溶液
C.c(H+)=c(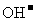 )
)
D.pH=3的酸与pH=11碱等体积混合后的溶液
1.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是 ( )
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com