
4.下列有关金属及其合金的说法不正确的是
A.目前我国流通的硬币是由合金材料制造的
B.生铁、普通钢和不锈钢中的碳含量依次增加
C.镁在空气中燃烧发出耀眼的白光,可用于制作照明弹
D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
3.化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.MgO的熔点很高,可用于制作耐高温材料
D.电解MgCl2饱和溶液,可制得金属镁
2.《中华人民共和国食品安全法》于2009年月1日起实施。下列做法不利于食品安全的是
A.用聚氯乙烯塑料袋包装食品
B.在食品盐中添加适量的碘酸钾
C.在食品加工中科学使用食品添加剂
D.研发高效低毒的农药,降低蔬菜的农药残留量
1.下列叙述错误的是
A.合金材料中可能含有非金属元素
B.人造纤维,合成纤维和光导纤维都是有机高分子化合物
C.加热能杀死流感病毒是因为病毒的蛋白质受热变性
D.在车排气管上加装“催化转化器”是为了减少有害气体的排放
38.(4分)甲烷与氧气按一定比例混合后点燃生成CO、CO2和H2O,生成物总质量为18.4g,通过浓硫酸后,质量减少9g,求:
(1)原混合气体中甲烷和氧气的体积比为 ;
(2)写出这一燃烧反应的化学方程式为 。
37.(10分)恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+ 3H2(g) 2NH3(g);反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量为25%(体积分数)。则:
2NH3(g);反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量为25%(体积分数)。则:
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a的值为 ;
(2)原混合气体中,a∶b= ;
(3)原混合气体与平衡混合气体的总物质的量之比,n(始):n(平)= ;
(4)若把容器体积减小一半,则正反应速率变 ,逆反应速率变 。
(填“大”、“小”或“不变”)
36.(4分)将铜片和锌片用导线连接后同时插入200mL硫酸铜溶液中,相当长时间后将铜片和锌片取出、烘干、称量,质量比反应前少0.1g。则
(1)此过程中有 个电子通过了导线;
(2)原硫酸铜溶液的物质的量浓度为 mol/L。
35.(9分)已知A、B、C、D、E均为短周期元素,原子序数按A、E、B、C、D的顺序依次递增。A元素原子形成的离子就是一个质子;C原子的最外层电子数是次外层的3倍;C和D可形成两种固体化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物;由A、B、C三种元素可形成离子化合物X,X中A、B、C元素原子的物质的量之比为A∶B∶C=4∶2∶3;E原子最外层电子数是内层电子数的2倍。回答下列问题:
(1)请写出元素符号: B 、C 、D 、E ;
(2)写出C和D形成的淡黄色固体化合物的电子式 ;
(3)化合物X的名称为: ;
(4)由B、C元素组成元素原子质量比为B∶C=7∶12的化合物的化学式 ;
(5)由A、B、C、E四种元素按原子个数比为5∶1∶3∶1组成的化合物的水溶液与足量的NaOH溶液在加热时发生反应的离子方程式为 。
34.(4分)(1)请写出氢氧燃料电池以KOH溶液为电解质溶液时正极的电极反应式:
;
(2)请写出甲烷燃料电池以KOH溶液为电解质溶液时负极的电极反应式:
。
33.(4分)有下列各组微粒或物质:
A. 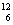 C和
C和 C B.CH3CH2CH2CH3和
C B.CH3CH2CH2CH3和 
C. D.
D. 和
和
(1)__________组两种微粒互为同位素;
(2)__________组两种物质属于同系物;
(3)__________组两种物质互为同分异构体;
(4)__________组两种物质是同一物质。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com