
18.据报道,最近摩托罗拉公司研发了一种甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可以连续使用一个月才充电一次。其电池反应为:2CH3OH+3O2+4OH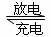 2CO32-+6H2O,则下列说法不正确的是( )
2CO32-+6H2O,则下列说法不正确的是( )
A.放电时CH3OH参与反应的电极为正极
B.放电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e-+8OH-=CO42-+6H2O
D.充电时每天生成1 molCH3OH转移6mol电子
17.下列反应的离子方程式书写正确的是 ( )
A.纯碱溶液呈碱性:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
B.向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全
A13++2SO42-+2Ba2++4OH=2BaSO4↓+A1O2+2H2O
C.碳酸钙溶于醋酸:CaCO3+2H+ Ca2++CO2↑+H2O
D.铜片跟稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O
16.HA是弱酸,用物质的量都是0.1mol的HA与NaA配制成1L溶液,已知其中c(A-)>c(Na+),有关该混合液的下列判断正确的是 ( )
A.c(H)>c(OH-) B.c(HA)>c(A-)
C.c(A-)+c(HA)=0.2mol/L D.c(A-)<0.1mol/L
15.下列说法中正确的是 ( )
A.将醋酸溶液稀释过程中,醋酸的电离程度增大,pH不增大
B.将氨水和烧碱溶液各稀释一倍,两者的c(OH-)均减少到原来的一半
C.体积相等,PH相同的盐酸和醋酸与过量的镁条反应,放出等量的氢气
D.常温下测得醋酸钠溶液的PH大于7,可以证明醋酸是弱酸
14.中和热测定实验中,下列操作一定会降低实验准确性的是 ( )
A.用滴定管量取酸碱的体积
B.NaOH溶液在倒入小烧杯时,有少量溅出
C.混合酸、碱溶液时,动作缓慢
D.测量HC1溶液的温度计用水洗净后才用来测NaOH溶液的温度
13.对于可逆反应:2A(g)+B(g) 2C(g);△H<0,下列各图正确的是 ( )
2C(g);△H<0,下列各图正确的是 ( )

12.下列说法,可以说明在固定条件下的密闭容器中,反应N2(g)+3H2 2NH3(g)已达到化学平衡状态的是 ( )
A.1个N≡N键断裂的同时,有6个N-H键断裂
B.3V顺(N2)=V逆(H2)
C.容器内混合气体的密度不再变化
D.容器内N2、H2、NH3的浓度比为1:3:2
11.下列说法正确的是 ( )
A.NH4BO2溶于水吸热,说明其溶于水不是自发过程
B.反应物的总能量高于生成物的总能量时发生放热反应
C.已知25℃,101Pa时,1molCH4完全燃烧生成CO2的水蒸气,放出的热量为802.3kJ,说明CH4的燃烧热为802.3kJ/mol
D.水力发电是将化学能转化为电能的过程
10.某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿。然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是 ( )

A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是负极,b点是正极
9.将2molSO2和2molSO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:
2SO2+O2(g) 2SO3(g),平衡时SO3为n mol。相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,平衡时SO3的物质的量大于n mol的是( )
2SO3(g),平衡时SO3为n mol。相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,平衡时SO3的物质的量大于n mol的是( )
A.2mol SO2+1 mol O2 B.4mol SO2+1molO2
C.2mol SO2+1mol O2+2mol SO3 D.3mol SO2+0.5mol O2+1molSO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com