
23.(6分)在50mLH2O2水溶液中加入2g二氧化锰,在标准状况下放出气体的体积与时间的关系如下图所示:

(1)该的反应化学方程式为 。
(2)若溶液的体积保持50mL不变,则在前五分钟H2O2的平均反应速率为 mol/(L·min)。
(3)试解释A、B、C各点所表示的反应速率变化的原因 。
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 (填化学式)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)
A.蒸馏 B.过滤 C.萃取 D.分液
(3)加入的足量试剂②是 (填化学式)。
(4)写出由无水MgCl2制取金属镁的化学方程式 。
(一)在海水提镁的过程中如何实现对镁离子的富集?
有三个学生提出自己的观点。
学生甲的观点:直接往海水中加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
通过分析比较你认为学生 的观点正确(填学生序号),简述理由: 。
21.(3分)以前人们发现把绿色的柠檬放在用煤油炉加温的帐篷里,可使其快速成熟,于是认为适当的温度是催熟柠檬的条件,但当把煤油炉换成暖气设备时,却没有得到预期的催熟效果,后来人们研究后断定催熟的因素是煤油未完全燃烧的气体中的一种成分。
(1)你认为上述有催熟性能的物质最有可能是下列中的 (选填编号)。
①甲烷 ②乙烯 ③苯 ④CO
(2)若要证实你的猜想,可将煤油未完全燃烧的气体收起来之后,通入 溶液。若观察到
现象,你的猜想可得到初步证实。
22.(12分)目前世界上60%的镁是从海水中提取的,下图是某工厂从海水中提取镁的主要步骤。学生就这个课题展开了讨论。
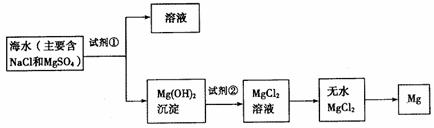
学生就这个课题提出了以下问题:
20.几种短周期元素的原子半径及主要化合价见下表:
|
元素代号 |
K |
L |
M |
Q |
R |
T |
N |
|
原子半径/nm |
0.183 |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
0.152 |
|
主要化合价 |
+1 |
+2 |
+3 |
+6,-2 |
+2 |
-2 |
+1 |
下列叙述正确的是 ( )
A.K、L、M三种元素的金属性逐渐增加
B.在RCl2分子中,各原子均满足8电子的稳定结构
C.Q元素的最高价氧化物为电解质,其水溶液能够导电
D.K在T单质中燃烧所形成的化合物中含有非极性共价键和离子键
第Ⅱ卷(非选择题 共50分)
19.镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应为Mg+2H++H2O2=Mg2++2 H2O。关于该电池说法正确的是 ( )
A.镁合金电源负极,发生还原反应 B.放电时H2O2在正极得电子,被还原
C.负极反应式为:Mg-2e-=Mg2+ D.放电时正极附近溶液酸性增强
18.某学生进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖。他的操作如下:取少量纯蔗糖加水配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟,冷却;在冷却后的溶液中加入银氨溶液,在水浴加热。实验结果没有银镜产生。其原因是 ( )
A.蔗糖尚未水解
B.蔗糖水解的产物是没有葡萄糖
C.加热时间不够
D.煮沸后的溶液中没有加碱,以中和作催化剂的酸
17.某混合物由乙酸和乙酸乙酯两种组分按一定比例组成,其中氢元素的质量分数为 ,则该混合物中氧元素的质量分数为 ( )
,则该混合物中氧元素的质量分数为 ( )
A.64% B.40% C.72% D.60%
16.下列关于元素周期表的叙述,不正确的是 ( )
A.ⅡA族中无非金属元素 B.Ⅷ族中所含元素种类最多
C.o族中无金属元素 D.金属元素和种类比非金属元素多
15.下列关于元素性质的有关叙述中不正确的是 ( )
A.C、N、O、F的原子半径依次减小
B.KOH、NaOH、LiOH的碱性逐渐减弱
C.P、S、Cl、Ar的最高正价依次升高
D.Na、Mg、Al、Si的最外层电子数依次增加
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com