
9.某温度时,测得纯水中c(H+)=2.4×10-7mol·L,则c(OH-)应为
A.(1.0×10-14/2.4×10-7)mol/L B.1.0×10-6mol/L
C.2.4×10-7mol/L D.无法确定
8.钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A.2 H+ +2e-=H2↑ B.Fe2++2e=Fe
C.2H2O+O4+4e=40H- D.Fe3++e-=Fe2+
7.将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸一段时间,以下叙述正确的是
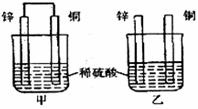
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
6.将0.1 mol/L醋酸溶液加水稀释,下列说法正确的是
A.溶液中c(H+)和c(OH-)都减小
B.溶液中c(H+)增大
C.醋酸电离平衡向左移动
D.溶液的pH增大
5.在25℃时,已知某弱电解质溶液A、强电解质溶液B、金属导体C的导电能力相同等温度升高到50℃时(假设溶液体积不变且不考虑溶质的挥发),则它们的导电能力的强弱关系为
A.A>B>C B.C>A>B C.A=B=C D.B>C>A
4.下列事实能说明醋酸是弱电解质的是
①醋酸与水能以任意比互溶 ②醋酸溶液能导电
③醋酸溶液中存在醋酸分子 ④0.1 mol/L醋酸的pH比0.1 mol/L盐酸的pH大
⑤醋酸能和碳酸钙反应放出CO2 ⑥0.1 mol/L醋酸钠溶液pH=8.9
A.②⑥ B.③④⑥ C.③④⑤⑥ D.①②
3.在碳酸溶液中,可发生如下电离:
H2CO3 H++
H++ ,
,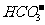
 H++
H++ ,若改变外界条件使得上述两个电离平衡均向右移动,则移动后,
,若改变外界条件使得上述两个电离平衡均向右移动,则移动后, 的物质的量浓度
的物质的量浓度
A.一定增大 B.可能增大也可能减小
C.一定减小 D.以上答案都不对
2.下列叙述正确的是
A.液态HCl、固态NaCl均不导电,所以二者均为非电解质
B.NH3、SO3的水溶液均导电,所以NH3、SO3是电解质
C.铜丝、石墨均导电,所以它们是电解质。
D.蔗糖、酒精在水溶液中或熔融时均不导电,所以它们是非电解质
1.下列变化过程中,是吸热反应的是
A.H+ H→H2 B.H+Cl→HCl C.I2→I+I D.S+O2-SO2
25、(16分)在实验室制取乙烯时,常因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气和炭黑。
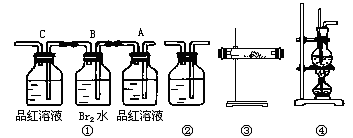
(1)写出该副反应的化学方程式(已知产物中CO2和C等量)
______ ____ __。
(2)用编号为①-④的实验装置设计一个实验,以验证上述反应混合气体中含CO2、SO2和水蒸气。所用装置的连接顺序(按产物气流从左到右的流向):______→______→______→______(填序号)
(3)实验的装置①中,A瓶的现象是____________;结论为____________B瓶溶液作用为____________。
(4)装置③中加的固体药品是___________以验证混合气体中有______。装置②中盛的溶液是__________。
(5)简述装置①在整套装置中位置的理由
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com