
11.改变下列条件,可以提高反应物中的活化分子百分数的是( )
A.降低温度 B.增大压强 C.使用催化剂 D.增大反应物浓度
10.下列事实不能用勒夏特利原理来解释的是:( )
A.用排饱和食盐水法收集氯气
B.加催化剂使N2和H2在一定条件下转化为NH3
C.增大压强,有利于SO2和O2反应生成SO3
D.在Fe3++3SCN- Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
9.某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)  2C(g)达到平衡时,测得A、B、C物质的量之比为2:2:1。若保持温度不变,以2:2:1的物质的量之比再充入A、B、C,下列判断正确的是( )
2C(g)达到平衡时,测得A、B、C物质的量之比为2:2:1。若保持温度不变,以2:2:1的物质的量之比再充入A、B、C,下列判断正确的是( )
A.平衡向逆反应方向移动 B.平衡不会发生移动
C.C的质量分数增大 D.C的质量分数可能减小
8.下图所示为8000C时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )
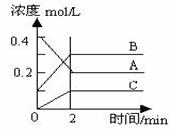
A.A是反应物
B.前2 min A的分解速率为0.1mol•L-1•min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.达平衡后,若增大压强,平衡向逆反应方向移动
7.某温度下,密闭容器中发生反应aX(g)  bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是( )
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是( )
A.可逆反应的化学计量数数:a>b+c
B.压缩容器的容积时,v正增大,v逆减小
C.达到新平衡时,物质X的转化率减小
D.达到新平衡时,混合物中Z的质量分数增大
6.一定条件下反应mA(g)+ nB(g)  pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是 ( )
pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是 ( )
A.2、6、3、5 B.3、1、2、2 C.3、1、2、1 D.1、3、2、2
5.反应2A(g) 2B(g)+C(g);正反应吸热,达平衡时,要使v正降低、c(A)增大,应采取的措施是( )
2B(g)+C(g);正反应吸热,达平衡时,要使v正降低、c(A)增大,应采取的措施是( )
A.加压 B.减压 C.减小c(B) D.降温
4.在容积固定的4L密闭容器中,进行可逆反应:X(g)+2Y(g)  2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图所示。则图中阴影部分面积表示
( )
2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图所示。则图中阴影部分面积表示
( )

A.X的浓度的减少 B.Y物质的量的减少
C.Z的浓度的增加 D.X 物质的量的减少
3.本题列举的四个选项是4位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
A.化学反应速率理论是研究怎样在一定时间内快出产品
B.化学平衡理论是研究怎样使用有限原料多出产品
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使原料尽可能多地转化为产品
2.在一个密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为:0.2mol/L, 0.2mol/L,0.2mol/L,当反应达到平衡时,可能出现的数据是 ( )
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为:0.2mol/L, 0.2mol/L,0.2mol/L,当反应达到平衡时,可能出现的数据是 ( )
A.c (SO3)=0.4mol/L B.c (SO2)=c (SO3)=0.15mol/L
C.c(SO2)=0.25mol/L D.c (SO2)+c (SO3)=0.5mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com