
9.下列电子式中,正确的是 ( )
A. B.
B.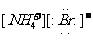
C.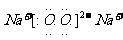 D.
D.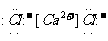
8.下列说法正确的是(NA为阿伏加德罗常数) ( )
A.124 g P4含有P-P键的个数为4NA
B.12 g石墨中含有C-C键的个数为2NA
C.12 g金刚石中含有C-C键的个数为2NA
D.60gSiO2中含Si-O键的个数为2NA
7.关于晶体的下列说法正确的是 ( )
A.只要含有金属阳离子的晶体就一定是离子晶体
B.离子晶体中一定含金属阳离子
C.在共价化合物分子中各原子都形成8电子结构
D.分子晶体的熔点不一定比金属晶体熔点低
6.关于化学键或晶体类型的下列叙述中,错误的是 ( )
A.非金属元素间形成的化合物不可能有离子键
B.离子化合物中可能含有极性共价键或非极性共价键
C.同族元素的氧化物可以形成不同类型的晶体
D.不同族元素的氧化物可以形成相同类型的晶体
5.下列叙述正确的是 ( )
A.构成分子晶体的粒子中一定含有共价键
B.在离子晶体中不可能存在非极性键
C.离子化合物中可能含有共价键
D.在原子晶体中不可能存在极性共价键
4.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是 ( )
A.金属性:Y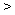 Z
B.氢化物的沸点:
Z
B.氢化物的沸点: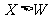
C.离子的还原性:X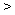 Y D.离子半径:
Y D.离子半径: 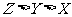
3.下列物质性质的变化规律,与键的键能大小无关的是 ( )
A. 、
、 、
、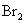 、
、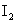 的熔点、沸点逐渐升高
的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.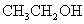 、
、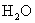 、
、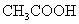 与Na反应由难到易
与Na反应由难到易
2.下列说法中正确的是 ( )
A.含有非极性共价键的化合物分子一定是非极性分子
B.原子晶体中只存在非极性共价键
C.冰主要是水分子通过氢键作用而形成的分子晶体
D.若元素R的含氧酸的酸性大于元素Q的含氧酸的酸性,则非金属性R大于Q
1.下列说法不正确的是 ( )
A.任何化学反应都伴随有能量变化
B.反应物总能量低于生成物的总能量时,该反应不能发生
C.反应物总能量高于生成物总能量时,发生放热反应
D.化石燃料在地球上的蕴藏量是有限的,而且又都是非再生能源
24.(10分)A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下各物质之间的相互转化关系如下图(图中部分产物未列出):
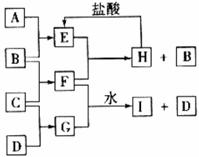
请填写下列空白
(1)A是 ,C是 。(写化学式)
(2)H与盐酸反应生成E的化学方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D的离子方程式是 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com