
26.(1)(4分)已知硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在催化剂作用下可发生氧化还原反应,生成高锰酸钾、硫酸钾和硫酸。
①配平并完成化学反应方程式:
MnSO4
+ K2S2O8
+ 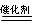 KMnO4 + K2SO4 + H2SO4
KMnO4 + K2SO4 + H2SO4
②当生成1mol高锰酸钾时,共有 mol电子转移。
(2)(9分) 向Ca(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如图所示,试回答:
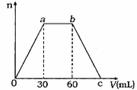
①a点之前反应的离子方程式为 ;
②c点的二氧化碳体积是 mL;
③混合稀溶液中Ca(OH)2和NaOH的物质的量之比为 。
13.300℃时,将等物质的量的CO、H2、CO2、H2O组成的混合气体共a mol,置于装有足量Na2O2的密闭容器中,用电火花连续作用,充分反应后,下列说法不正确的是
A.Na2O2的质量增加15a g
B.剩余气体的物质的量为 mol
mol
C.剩余固体中 ∶
∶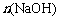 = 1∶2
= 1∶2
D.反应过程中共转移a mol 电子
第Ⅱ卷 非选择题(共174分)
12.下列反应的离子方程式书写正确的是
A.铁屑溶于足量稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O
C.金属钠溶于足量水中:2Na+2H+=2Na++H2↑
D.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
11.下列是某学生自己总结的一些规律,其中正确的是
A.一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物
B.气体的体积主要由分子间的距离决定,所以相同数目的分子具有相同的体积
C.已知K2O、K2O2、KO2的名称依次是氧化钾、过氧化钾、超氧化钾。那么BaO2的名称是过氧化钡
D.准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容。可以快速配制1000mL氯化钾溶液
10.下列各组离子在指定溶液中能大量共存的是
A.在能使石蕊试纸变蓝色的溶液中:Na+ 、AlO2-、S2-、SO42-
B.由水电离的H+浓度c(H+)= 10-12mol·L-1的溶液中:Cl-、CO32-、NH4+、SO32-
C.在加入铝粉能产生H2的溶液中:NH4+ 、Na+ 、Fe2+ 、NO3-
D.pH=2的溶液中:Na+ 、SO42-、NO3-、AlO2-
9.把NaHCO3和NaOH的混合物放在密闭容器中加热。关于混合物加热前后消耗盐酸的量,下列判断正确的是
A.加热前消耗的多 B.加热后消耗的多
C.加热前后一样多 D.当NaOH适量时才会一样多
8.高铁酸钾是一种理想的绿色水处理剂,工业上可通过如下反应制得
Fe(OH)3 + ClO-+OH- -FeO42-+ Cl-+ H2O(未配平),在上述反应中
A.FeO42-是还原产物 B.ClO-是还原剂
C.1 mol Fe(OH)3得到3mol电子 D.配平后OH- 的化学计量数为4
7.设NA表示阿伏伽德罗常数的值,下列说法正确的是
A.常温常压下,通过分解反应制取1molO2时,转移的电子总数都为4NA
B.在标准状况下,NA个H2O分子所占体积为22.4L
C.在标准状况下,以任意比例混合的CH4与CO2 的混合物22.4L所含有的分子数为NA
D.常温常压下,28g氮气含有的核外电子数为10 NA
6.今有一固体化合物X,X本身不导电,但熔化状态或溶于水中能够导电,下列关于该化合物X的说法中正确的是
A.X可能为非电解质 B.X一定为电解质
C.X只能为盐类 D.X可以是任何化合物
30.(12分)A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R'为烷基)。
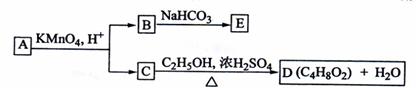
回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为_____________;
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是__________ _,反应类型为_____________:
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________________
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有__________种,其相应的结构简式是__________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com