
5.下列反应中,调节反应条件或反应物的量以后,反应产物不会改变的是 ( )
A.钠与氧气 B.硫酸与铝片
C.盐酸与铁粉 D.稀硝酸与铁粉
4.能实现下列物质间直接转化的元素是 ( )

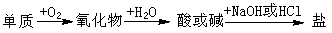
 A.硅 B.硫 C.铜 D.铁
A.硅 B.硫 C.铜 D.铁
3. 在通常条件下,下列各组物质的性质排列正确的是 ( )
在通常条件下,下列各组物质的性质排列正确的是 ( )
 A.熔点:CO2>KCl>SiO2 B.水溶性:HCl>H2S>SO2
A.熔点:CO2>KCl>SiO2 B.水溶性:HCl>H2S>SO2
 C.还原性:HF>HCl>HBr>HI
D.热稳定性:HF>H2O>NH3
C.还原性:HF>HCl>HBr>HI
D.热稳定性:HF>H2O>NH3
2.下列物质中主要成分不是二氧化硅的是 ( )
A.水泥 B.水晶 C.玛瑙 D.硅石
1.下列有关物质分类或归类正确的是 ( )
①混合物:碱石灰、水玻璃、双氧水 ②化合物:CaCl2、NaOH、HD
③电解质:明矾、AlCl3、氯化银 ④同素异形体:C60、金刚石、石墨
A.③④ B.②③④ C.①③④ D.①④
29.(17分)
苹果醋是由苹果发酵而成的酸性饮品,具有解毒、减肥等功效。苹果酸(A)是这种饮料中的主要酸性物质。已知:下列有关苹果酸(A)的转化关系中,B能使溴的四氯化碳溶液褪色。回答下列问题:
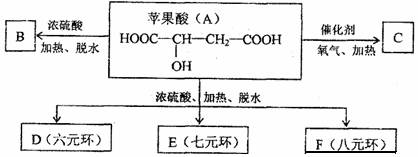
(1)苹果酸分子中所含的官能团名称是
(2)苹果酸不能发生的反应有 (填写序号)
①加成反应 ②酯化反应 ③加聚反应 ④氧化反应 ⑤消去反应
(3)写出B的结构简式 ;F的分子式
(4)写出A→D的方程式
(5)苹果酸(A)有多种同分异构体,写出符合下列条件的两种同分异构体的结构简式,条件是:①在一定条件下,能发生银镜反应;②能与乙醇发生酯化反应;③能与苯甲酸发生酯化反应;④分子中同一碳原子不能连有两个羟基。
28.(15分)
为节省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、硫酸铜溶液、直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器,进行巧妙构思,以“接力”的方式,设计了比较铜与锌金属活动性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜、锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是 ;甲同学设计思路是 。
(2)乙同学接着甲的实验,向烧杯中滴加 溶液,进而观察到的现象是 , 。乙同学作出锌、铜金属活动性相对强弱所依据的原理是 , 。
(3)丙同学使用直流电源和石墨电极组装电解装置,向乙同学实验后的溶液中补充了必要的试剂(作电解液)。电解过程中所发生的化学反应方程式为 。观察到的实验现象主要有 。
(4)请你再单独设计一个简单的实验(仪器、试剂任选),探究和证实铜锌元素金属活动性相对强弱(简要说明操作)
。
27.(16分)
下列物质间在一定条件下可以实现如图所示的一系列变化,其中A是中学化学中常见的单质气体,可使带火星木条燃烧的更旺,且实验室可以用固体X和黑色固体Y来制备气体A;固体B为混合物,白色沉淀D不溶于稀硝酸;E的焰色反应为紫色(透过蓝色钴玻璃观察)。请填写下列空白:
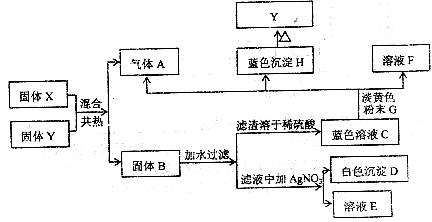
(1)写出下列物质的化学式:
X ,Y ,A ,D ,
G ,H 。
(2)写出蓝色溶液C与淡黄粉末G反应的化学方程式
(3)写出X与Y共热的化学方程式:
Y的作用是 ,据此你可得出的结论是 。
26.(12分)
新华网武汉2008年5月3日电,武汉两家5口人同时发生罕见的铊中毒后造成1人死亡,2人病危。铊(Tl)是某超导体材料的组成元素之一,与铜同族。Tl3+与Ag在酸性介质中发生反应Tl3++2Ag===Tl++2Ag+,
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第 周期第 族。
(2)铊与下列元素位于同主族,该元素是
A.硼 B.氮 C.碳 D.氟
(3)下列推断正确的是
A.单质的还原性:Tl>Al B.原子半径:Al>Tl
C.碱性:Al(OH)3>Tl(OH)3 D.氧化性:Tl3+>Al3+
E.Tl+最外层只有1个电子 F.Tl能形成+3价和+1价的化合物
13.2008年奥运会主场鸟巢被《泰晤士报》评为全球最强悍的工程,鸟巢运用了高强度、高性能的钒氯合金高新钢和884块ETFE膜,并采用新一代的氮化镓高亮度LED材料。下列说法正确的是 ( )
A.合金的熔点通常高于组分的熔点,硬度也小于组分的硬度
B.已知Ga处于IIIA族,可推测氮化镓的化学式为Ga3N2

 C.ETFE膜 [ CH2-CH2-CF2-CF2 ]n 是由两种单体形成的膜
C.ETFE膜 [ CH2-CH2-CF2-CF2 ]n 是由两种单体形成的膜
D.工业上可以用金属铝与V2O5在常温下冶炼钒,铝做还原剂
第Ⅱ卷(非选择题)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com