
4ЃЎЯТСаГ§ШЅдгжЪЕФЗНЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎГ§ШЅN2жаЕФЩйСПO2ЃКЭЈЙ§зЦШШЕФCuOЗлФЉЃЌЪеМЏЦјЬх
ЁЁЁЁЁЁ BЃЎГ§ШЅFeCl2ШмвКжаЕФЩйСПFeCl3ЃКМгШызуСПЬњаМЃЌГфЗжЗДгІКѓЃЌЙ§ТЫ
ЁЁЁЁЁЁ CЃЎГ§ШЅCO2жаЕФЩйСПHCIЃКЭЈШыNa2CO3ШмвКЃЌЪеМЏЦјЬх
ЁЁЁЁЁЁ DЃЎГ§ШЅKClШмвКжаЕФЩйСПMgCl2ЃКМгШыЪЪСПNaOHШмвКЃЌЙ§ТЫ
3ЃЎТШЛЏЬњШмвКгыЧтбѕЛЏЬњНКЬхОпгаЕФЙВЭЌаджЪЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЗжЩЂжЪПХСЃжБОЖЖМдкl-100nmжЎМф
ЁЁЁЁЁЁ BЃЎФмЭИЙ§АыЭИФЄ
ЁЁЁЁЁЁ CЃЎМгШШеєИЩЁЂзЦЩеКѓЖМгабѕЛЏЬњЩњГЩ
ЁЁЁЁЁЁ DЃЎГЪКьКжЩЋ
2ЃЎЙигкЮяжЪЕФЗжРре§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎSO2ЁЂCO2ЁЂCOЁЂNO2ЖМЪЧЫсадбѕЛЏЮя
ЁЁЁЁЁЁ BЃЎNa2OЁЂNa2O2ЁЂFe2O3ЁЂCuOЖМЪЧМюадбѕЛЏЮя
ЁЁЁЁЁЁ CЃЎHCIЁЂHClOЁЂHClO3ЁЂHClO4ЖМЪЧЧПЫс
ЁЁЁЁЁЁ DЃЎNaOHЁЂKOHЁЂBa(OH)2ЁЂCa(OH)2ЖМЪЧЧПМю
1ЃЎЯТСаЪЕбщВйзїжаЃЌвЛАуЧщПіЯТВЛгІИУЯрЛЅНгДЅЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎгУНКЭЗЕЮЙмЯђЪдЙмжаЕЮвКЬхЪБЃЌЕЮЙмМтЖЫгыЪдЙмФкБк
ЁЁЁЁЁЁ BЃЎЯђШнСПЦПжазЊвЦвКЬхЪБЃЌЪЙгУЕФВЃСЇАєгыШнСПЦПОБФкБк
ЁЁЁЁЁЁ CЃЎЙ§ТЫВйзїжаЃЌТЉЖЗФЉЖЫгыГаНгТЫвКЕФЩеБФкБк
ЁЁЁЁЁЁ DЃЎЪЕбщЪвНЋHClЦјЬхШмгкЫЎЪБЃЌТЉЖЗПкгыЫЎУц
33ЃЎ(8Зж)[ЛЏбЇ--гаЛњЛЏбЇЛљДЁ]
вдЯТЪЧЩњВњВнЫсЕФвЛЯЕСаЗДгІЃЎ

вбжЊBЕФЯрЖдЗжзгжЪСПБШAЕФДѓ79ЁЃ
(1)ЧыаДГіCКЭFЕФНсЙЙМђЪНЃКC_________ЃЌF_________ЁЃ
(2)ВнЫсПЩгыввЖўДМЗДгІЩњГЩвЛжжЛЗзДЕФѕЅЃЌаДГіетИіЗДгІЕФЛЏбЇЗНГЬЪН___________ЁЃ
(3)ВнЫсПЩгыввЖўДМЗДгІЩњГЩвЛжжИпЗжзгЛЏКЯЮяЃЌЪдаДетжжИпЗжзгЛЏКЯЮяЕФСДНк_____ЁЃ
(4)C9H8O4гыВнЫсЪєгкЭЌвЛРрЮяжЪЃЌЪдаДГіЗћКЯЯТСаЬѕМўЕФЭЌЗжвьЙЙЬхЪ§ЪЧ________ЁЃ
ЂйЪєгкЗМЯузхЛЏКЯЮя
Ђк1molетжжЮяжЪгызуСПЕФЬМЫсЧтФЦШмвКЗДгІПЩВњЩњ2molЕФЖўбѕЛЏЬМ
ЂлВрСДЩЯУЛгаМзЛљ
32ЃЎ(8Зж)[ЛЏбЇ--ЮяжЪНсЙЙгыаджЪ]
(1)ЕкЖўжмЦкжаЮДГЩЖдЕчзгЪ§зюЖрЕФдЊЫиCгыЕкШ§жмЦкЕквЛЕчРыФмзюаЁЕФдЊЫиDПЩвдаЮГЩD3CЃЌD3CгіЫЎВњЩњЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЩЋЕФЦјЬхЃЌдђD3CгыбЮЫсЗДгІЕФЛЏбЇЗНГЬЪНЮЊ___________________________ЁЃ
(2)юб(Ti)ЕФдзгађЪ§ЮЊ22ЃЌЦфМлЕчзгХХВМЪНЮЊ________ЁЃюбЕФЛЏКЯЮяTiCl3ЁЄ6H2O(ЯрЖдЗжзгжЪСПЮЊ262.5)ХфЮЛЪ§ЮЊ6ЃЌШЁИУОЇЬх26.25gХфГЩШмвКЃЌМгШызуСПAgNO3ШмвКЃЌЙ§ТЫЁЂЯДЕгЁЂКцИЩЁЂГЦжиЃЌГСЕэЮЊ28.70gЃЌдђИУОЇЬхЕФЛЏбЇЪНгІБэЪОЮЊ_________ЃЌОЇЬхжаКЌТШдЊЫиЕФЮЂСЃгыЦфЫћЮЂСЃМфЕФзїгУСІЪЧ_________ЁЃ
31ЃЎ(8Зж)[ЛЏбЇ--ЛЏбЇгыММЪѕ]
ВФСЯПЦбЇЪЧНќФъРДгыЛЏбЇгаЙиЕФПЦбЇбаОПЕФШШЕуЁЃФГаТаЭЮоЛњЗЧН№ЪєВФСЯKгЩСНжжЗЧН№ЪєдЊЫизщГЩЃЌЫќЪЧвЛжжГЌгВЮяжЪЃЌОпгаФЭФЅЁЂФЭИЏЪДЁЂПЙРфШШГхЛїЁЂПЙбѕЛЏЕФЬиадЃЌЫќЪЧвджабЇЛЏбЇжаЕФГЃМћЮяжЪЮЊдСЯРДЩњВњЕФЃЌЯТЭМЫљЪОЮЊЦфЩњВњЙ§ГЬЃЌЦфжаащЯпПђФкзЊЛЏЪЧЮЊЬНОПCЕФзщГЩЖјЩшЃЌGЁЂFЁЂHОљФбШмгкЫЎЃЌЧвЮЊАзЩЋЗлФЉЃЛЭМжаГ§MЁЂK(ОљКЌAдЊЫи)ЭтОљЮЊжабЇЛЏбЇГЃМћЮяжЪЃК
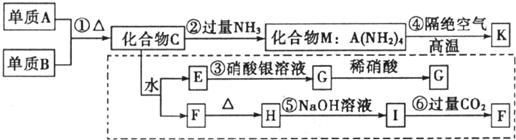
(1)аДГіЛЏбЇЪНЃКЕЅжЪB_________ЃЌЛЏКЯЮяF_________ЁЃ
(2)аДГіЯТСаЗДгІЕФРызгЗДгІЗНГЬЪНЃК
ЗДгІЂл__________________________ЃЌЗДгІЂн__________________________ЁЃ
(3)аДГіЗДгІЂмЕФЛЏбЇЗНГЬЪН____________________________________ЁЃ
30ЃЎ(12Зж)ФГПЮЭтЛюЖЏаЁзщЩшМЦСЫвдЯТЪЕбщЗНАИбщжЄAgгыХЈЯѕЫсЗДгІЕФЙ§ГЬжаПЩФмВњЩњNOЁЃЦфЪЕбщСїГЬЭМШчЯТЃК
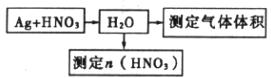
ЕквЛВНЃКВтЖЈЯѕЫсЕФЮя
ЗДгІНсЪјКѓЃЌДгЯТЭМBзАжУжаЫљЕУ100mLШмвКжаШЁГі25mLШмвКЃЌгУ0.1 ЕФNaOHШмвКЕЮЖЈЃЌгУЗгЬЊзїжИЪОМСЁЃВтЕУдкBШнЦїжаЩњГЩЯѕЫсЕФЮяжЪЕФСПЮЊ0.008molЃЌдђAgгыХЈЯѕЫсЗДгІЙ§ГЬжаЩњГЩЕФNO2ЬхЛ§ЮЊ__________mL(елЫуГЩБъзМзДПі)ЁЃ
ЕФNaOHШмвКЕЮЖЈЃЌгУЗгЬЊзїжИЪОМСЁЃВтЕУдкBШнЦїжаЩњГЩЯѕЫсЕФЮяжЪЕФСПЮЊ0.008molЃЌдђAgгыХЈЯѕЫсЗДгІЙ§ГЬжаЩњГЩЕФNO2ЬхЛ§ЮЊ__________mL(елЫуГЩБъзМзДПі)ЁЃ
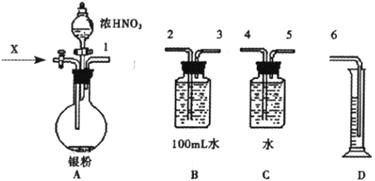
ЕкЖўВНЃКВтЖЈNOЕФЬхЛ§
(1)ДгЩЯЭМЫљЪОЕФAзАжУжаНјааAgгыХЈЯѕЫсЗДгІЪЕбщЃЌXЪЧдкЗДгІЧАЭЈШыЕФвЛжжЦјЬхЃЌЯТСаЦјЬхжаЗћКЯЬѕМўЕФЪЧ__________
ЂйЕЊЦјЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ ЂкЧтЦјЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ ЂлПеЦјЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ ЂмТШЛЏЧт
(2)бЁгУЩЯЭМЫљЪОвЧЦїзщКЯвЛЬзПЩгУРДВтЖЈЩњГЩNOЬхЛ§ЕФзАжУЃЌЦфКЯРэЕФСЌНгЫГађЪЧ____________________(ЬюИїЕМЙмПкБрКХ)ЁЃ
(3)дкВтЖЈNOЕФЬхЛ§ЪБЃЌШєСПЭВжаЫЎЕФвКУцБШМЏЦјЦПЕФвКУцвЊЕЭЃЌДЫЪБгІНЋСПЭВЕФЮЛжУ__________(ЁАЯТНЕЁБЛђЁАЩ§ИпЁБ)ЃЌвдБЃжЄСПЭВжаЕФвКУцгыМЏЦјЦПжаЕФвКУцГжЦНЁЃ
ЕкШ§ВНЃКЦјЬхГЩЗжЗжЮі
ШєЪЕбщВтЕУNOЕФЬхЛ§ЮЊ112mlЃЎ(вбелЫуЕНБъзМзДПі)ЃЌдђAgгыХЈЯѕЫсЗДгІЕФЙ§ГЬжа__________(ЬюЁАгаЁБЛђЁАУЛгаЁБ)NOВњЩњЃЌзїДЫХаЖЯЕФвРОнЪЧ__________________ЁЃ
[бЁзіВПЗж]
ЙВ8ИіЬтЃЌПМЩњДгжабЁдё2ИіЮяРэЬтЁЂ1ИіЛЏбЇЬтКЭ1ИіЩњЮяЬтЃЌдкД№ЬтПЈЙцЖЈЧјгђзїД№ЁЃ
29ЃЎ(16Зж)AЁЂBЁЂCЁЂDЁЂEЁЂFСљжжЮяжЪЕФЯрЛЅзЊЛЏЙиЯЕШчЯТЭМЫљЪО(ЗДгІЬѕМўЮДБъГі)ЃЌЦфжаЗДгІЂйЪЧжУЛЛЗДгІЁЃ
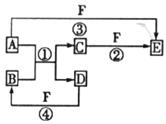
(1)ШєAЪЧГЃМћЕФН№ЪєЕЅжЪЃЌDЁЂFЪЧЦјЬЌЕФЕЅжЪЃЌЗДгІЂйдкЫЎШмвКжаНјааЁЃЪдЭЦВтA__________ЁЂD__________(ЬюЛЏбЇЪН)ЃЌEЕФЫЎШмвКЯдЫсадЃЌЦфдвђЪЧ(гУРызгЗНГЬЪНРДБэЪО)____________________ЃЛвбжЊ1g DгыFЗДгІЩњГЩBЪБЗХГіСЫ92.3kJЕФШШСПЃЌаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН____________________ЁЃ
(2)ШєAЁЂDЮЊЖЬжмЦкдЊЫиЕФЕЅжЪЃЌЧвЫљКЌдЊЫиЕФдзгађЪ§AЪЧDЕФ2БЖЃЌдзгзюЭтВуЕчзгЪ§DЪЧAЕФ2БЖЃЌЂлЂмЗДгІжаЖМгаКьзиЩЋЦјЬхЩњГЩЃЌЂкЂлЂмЗДгІжаЕФВПЗжВњЮявбОТдШЅЁЃAжадЊЫидкжмЦкБэжаЕФЮЛжУЪЧ____________________ЃЛBЕФЕчзгЪНЪЧ____________________ЃЛПђЭМжаЕФ4ИіЛЏбЇЗДгІжаFМШБэЯжбѕЛЏадгжБэЯжЫсадЕФЪЧ(ЬюађКХ)______________________________ЁЃ
28ЃЎ(14Зж)
(1)ЯТСаЫЕЗЈе§ШЗЕФЪЧ__________ЁЃ
ЂйдЕчГиЪЧНЋЕчФмзЊЛЏЮЊЛЏбЇФмЕФзАжУ
ЂкЯрЭЌжЪСПЕФЬњЗЂЩњЮќбѕИЏЪДКЭЮіЧтИЏЪДзюжезЊвЦЕчзгЕФЪ§ФПЯрЕШ
ЂлЕчНтОЋСЖЭЪБЃЌШєгУСђЫсЭШмвКзїЕчНтжЪШмвКЃЌЭРызгЕФХЈЖШВЛБф
ЂмгУЬњзїЕчМЋЃЌЕчНтЕЮгаЗгЬЊЕФБЅКЭЪГбЮЫЎЪБЃЌвѕМЋЧјВЛБфКь
ЂнбѕЛЏЛЙдЗДгІжавЛЖЈгаЕчзгзЊвЦ
ЂоН№ЪєЕФЛЏбЇИЏЪДЪЕжЪЪЧ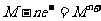 ЃЌЕчзгжБНгзЊвЦЕНбѕЛЏМС
ЃЌЕчзгжБНгзЊвЦЕНбѕЛЏМС
ЂпгУЖшадЕчМЋЕчНтCuSO4ШмвКвЛЖЮЪБМфКѓвѕМЋЮоЦјЬхЗХГіЃЌЯђШмвКжаМгШывЛЖЈСПЕФCuOПЩЪЙШмвКЛжИДЕНдХЈЖШ
(2)дквЛШнЛ§ЮЊ2 LЕФУмБеШнЦїМгШы0.2molN2КЭ0.6 molH2ЃЌдквЛЖЈЬѕМўЯТЗЂЩњШчЯТЗДгІЃК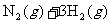

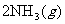
 ЃЌЗДгІжаNH3ЕФЮяжЪЕФСПХЈЖШЕФБфЛЏЕФЧщПіШчЯТЭМЃК
ЃЌЗДгІжаNH3ЕФЮяжЪЕФСПХЈЖШЕФБфЛЏЕФЧщПіШчЯТЭМЃК

ЂйИљОнЩЯЭМЃЌМЦЫуДгЗДгІПЊЪМЕНЦНКтЪБЃЌЦНОљЗДгІЫйТЪ ЮЊ__________
ЮЊ__________
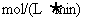 ЁЃ
ЁЃ
ЂкЗДгІДяЕНЦНКтКѓЃЌЕк5minФЉЃЌБЃГжЦфЫќЬѕМўВЛБфЃЌШєИФБфЗДгІЮТЖШЃЌдђNH3ЕФЮяжЪЕФСПХЈЖШВЛПЩФмЮЊ__________ЁЃ
aЃЎ0.20 molЃЏLЁЁ ЁЁЁЁ bЃЎ0.12 molЃЏLЁЁЁЁ ЁЁЁЁ cЃЎ0.10 molЃЏL ЁЁ ЁЁdЃЎ0.08 molЃЏL
ЂлЗДгІДяЕНЦНКтКѓЃЌЕк5minФЉЃЌБЃГжЦфЫќЬѕМўВЛБфЃЌШєжЛАбШнЦїЕФЬхЛ§ЫѕаЁвЛАыЃЌЦНКт__________вЦЖЏ(ЬюЁАЯђФцЗДгІЗНЯђЁБЁЂЁАЯђе§ЗДгІЗНЯђЁБЛђЁАВЛЁБ)ЃЌЛЏбЇЦНКтГЃЪ§__________(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
ЂмдкЕк5minФЉНЋШнЦїЕФЬхЛ§ЫѕаЁвЛАыКѓЃЌШєдкЕк8minФЉДяЕНаТЕФЦНКт(ДЫЪБNH3ЕФХЈЖШдМЮЊ0.25 molЃЏL)ЃЌЧыдкЩЯЭМжаЛГіЕк5minРДЕНДЫКѕКтЪБNH3ХЈЖШЕФБфЛЏЧњЯпЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com