

7.某有机物,因其酷似奥林匹克五环旗,科学家称其为奥林匹克烃(Olympiadane)下列有关奥林匹克烃的说法正确的是 ( )
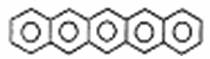
A.该有机物属于芳香族化合物,是苯的同系物
B.属于烃的衍生物
C.该物质的一溴代物有四种
D.符合通式CnH2n-6
6.有关有机物的下列说法中正确的是 ( )
A.含五个碳原子的有机物,分子中最多可形成四个碳碳双键
B.淀粉和纤维素互为同分异构体,因为它们的化学通式相同
C.分子式为C8H6O3的芳香族有机物分子中可能有羧基
D.根据蛋白质的变性原理,硫酸铜溶液可以作为外伤止血剂
5.将CH3COOC2H5放入H218O中,用酸作为催化剂,最终含有18O原子的物质及其结构简式表示方法正确的是 ( )
A.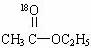 B.
B.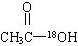
C.CH3CH218OH D.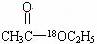
4.食品安全问题引起广泛关注。下列作法正确的是 ( )
A.用硫磺熏制白净的粉丝
B.用福尔马林保鲜海产品
C.用三聚氰胺作食品添加剂,以提升食品检测中的蛋白质含量指标
D.腌制食品中严格控制NaNO2的用量
3.以下反应最符合绿色化学原子经济性要求的是 ( )
A.乙炔与氯化氢合成氯乙烯
B.甲烷与氯气制备一氯甲烷
C.乙酸和乙醇反应生成乙酸乙酯
D.乙醇和浓硫酸混合制乙烯
2.下列各化合物的命名中正确的是 ( )
A.CH2=CH-CH=CH2 1,3一二丁烯 B.CH3CH2CH(OH)CH3 3一丁醇
C.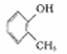 甲基苯酚 D.
甲基苯酚 D.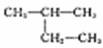 2-甲基丁烷
2-甲基丁烷
1.化学与生产生活密切相关,聚乙烯制成品在我们生活中常常用到,下列有关说法中正确的是 ( )
A.乙烯通过加聚反应可制得聚乙烯 B.聚乙烯制成品无毒,可无限制使用
C.聚乙烯可使酸性高锰酸钾溶液褪色 D.聚乙烯有固定的熔沸点
29.(14分)已知pH值为4-5的条件下, 几乎不水解,而
几乎不水解,而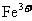 几乎完全水解。某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(
几乎完全水解。某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(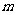 )以及电极上产牛气体的体积(
)以及电极上产牛气体的体积(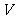 mL标准状况)来测定Cu的相对原子质量,过程如下图所示:
mL标准状况)来测定Cu的相对原子质量,过程如下图所示:
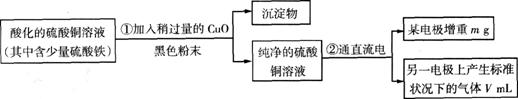
回答下列问题:
(1)加入CuO的作用是_______________________________________。
(2)步骤②中所用的部分仪器如下图所示,则A连接直流电源的___________极。
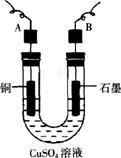
(3)电解开始后,在U形管中可以观察到的现象有__________________________,_______________________。电极B的电极反应方程式为_____________________。
(4)下列实验操作中必要的是___________(填写字母)。
A.称量电解前的电极的质量
B.电解后,电极在烘干称量前,必须用蒸馏水冲洗
C.刮下电解后电极上析出的铜,并清洗,称量
D.电解后烘干称重的操作中必须按“烘干-称量-再烘干-再称量”进行
E.在有空气存在的情况下,烘干电极必须用低温烘干的方法
(5)铜的相对原子质量为___________(用带有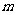 、
、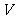 的计算式表示)。
的计算式表示)。
28.(14分)a、b、c、d、e为原子序数依次增大的五种短周期元素。a与b能形成原子数之比为1︰1和2︰1的两种常见的液态化合物X、Y;在元素周期表中c与d的位置相邻,d的一种单质化学式为d4,易自燃,其分子结构为正四面体结构。试回答下列问题:
(1)化合物X能被酸性KMnO4溶液氧化,写出对应的离子方程式__________________。若有16 g气体生成,则转移电子的物质的量为_____________mol。
(2)c与b形成的化合物Z晶体类型为_____________;等物质的量的Z和d4的共价键数之比为_____________。
(3)3.1g d4在空气中完全燃烧放出Q kJ的热量,则d4燃烧热的热化学方程式为:____________________________________(用化学式表示各物质)。
(4)d与e能形成de3和de5两种化合物,其中各原子都满足8电子结构的化合物的电子式为_____________;de5能与水反应,生成两种常见的酸,其中一种为高沸点难挥发酸,请写出对应的化学方程式__________________。
27.(15分)
Ⅰ.在体积为5 L的恒温、恒容、密闭容器甲中,起始投入2 mol N2、3 mol H2,经过10s达到平衡,测得平衡时NH3的物质的量为0.8 mol。
Ⅱ.容器乙起始通入 molN2,
molN2, molH2,维持恒温、恒压到平衡,测得平衡时NH3的物质的量为1.2 mol。
molH2,维持恒温、恒压到平衡,测得平衡时NH3的物质的量为1.2 mol。
两平衡温度相同、相同组分的体积分数相同。
(1)容器甲10s内用H2表示的平均反应速率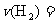 _____________,达平衡时N2的转化率
_____________,达平衡时N2的转化率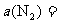 _____________。
_____________。
(2)下列哪些情况表明容器乙已达平衡状态_____________(填写字母)。
A.容器乙的气体密度不再变化
B.氢元素的质量不再变化
C.氮气的生成速率等于氨气的消耗速率
D.断裂1 mol N≡N键,同时断裂6 mol N-H键
(3)达平衡时甲容器的压强________乙容器的压强(选填“等于”、“大于”或“小于”)。
(4) __________mol,
__________mol,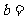 _________mol。
_________mol。
(5)达平衡时乙容器的体积为_____________L;起始时容器乙的压强是容器甲的压强的_____________倍。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com