

17.L-多巴是一种有机物,可用于帕金森综合症的治疗,其结构简式如下:
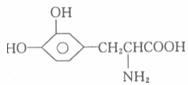
下列关于L-多巴的叙述中不正确的是 ( )
A.长期暴露在空气中易变质 B.既有酸性,又有碱性
C.一定条件下能发生聚合反应 D.分子中最多只有6个碳原子共平面
18.广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述信息,下列说法不正确的是 ( )
A.CaO2的水解产物是Ca(OH)2和H2O2
B.PCl3的水解产物是HClO和PH3
C.NaClO的水解产物之一是HClO
D.Mg3N2的水解产物是两种碱性物质
16.工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)===Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
某温度,压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是 ( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH恰好反应
15.进行化学实验或探究活动,都必须注意实验安全。下列实验操作合理的是( )
A.为防止试管破裂,加热固体高锰酸钾制氧气时,试管口应向下倾斜
B.进行SO2性质探究实验时,多余的SO2应排到实验室外
C.为防止药品污染,实验结束后,用剩的白磷可溶解于CS2后倒入垃圾箱
D.配制H2SO4溶液时,先在量筒中加一定体积的水,再在搅拌下慢慢加入浓H2SO4
14.对胶体稳定不起作用的是 ( )
A.胶体微粒直径介于溶液与浊液之间
B.胶体微粒具有吸附作用
C.丁达尔现象
D.布朗运动
13.下列离子反应方程式书写正确的是 ( )
A.在Ba(OH)2溶液中加入少量的硫酸氢钠溶液:
Ba2++2OH-+2H++SO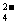 =BaSO4↓+2H2O
=BaSO4↓+2H2O
B.向次氯酸钙溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.标准状况下,将112mLCl2缓慢注入10mL 1mol·L-1的FeBr2溶液中:
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
D.向苯酚钠溶液中通入少量CO2气体:
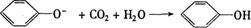 + HCO
+ HCO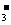
12.下列反应的ΔH表示的是中和热的是: ( )
A.H2SO4(aq) + Ba(OH)2(aq) == BaSO4(s) + 2H2O(l ); ΔH1
B.H2SO4(浓aq) + NaOH(aq) == Na2SO4(aq) + H2O(l); ΔH2
C.HCl(aq) + NaOH(aq) == NaCl(aq) + H2O(l); ΔH3
D.HAc(aq) + NaOH(aq) == NaAc(aq) + H2O(l); ΔH4
11.某无色澄清溶液与NH4HCO3在一定条件下作用能产生气体,则在此溶液中肯定能大量共存的离子组是 ( )
A. MnO4-、Mg2+、Cl-、SO42-
B.Na+、Ba2+、NO3-、SO42-
C.Cl-、Na+、K+、SO42-
D.K+、NO3-、SO42-、Al3+
10.设 NA表示阿伏加德罗常数的值。下列说法正确的是 ( )
A.常温常压下,100mL0. 1 mol·L-1,HCOOH 溶液中含 H+数目为 0. 0lNA
B.标准状况下,22 . 4L 氯仿所含的分子数为 NA
C.室温下,42 . 0g 乙烯和丙烯的混合气体中含有的碳原子数为 3NA
D.一定条件下,向密闭容器中加入l mol N2和3molH2,反应结束后,转移的电子数为6NA
9.Y元素的最高正价与最低负价的绝对值之差是4;Y元素可与M元素形成离子化合物,并在水中电离出电子层结构相同的阴.阳离子,则该化合物是 ( )
A.K2S B.Na2S C.Na2O D.KCl
8.能够使反应Cu+2H2O=Cu(OH)2↓+H2↑发生的是 ( )
A.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液
B.铜锌合金在潮湿的空气中发生电化学腐蚀
C.用铜片作阴.阳电极,电解硫酸钠水溶液
D.用铜片作阴.阳电极,电解硫酸铜水溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com