
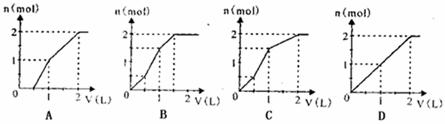
12.向含有1mol HCl和1mol MgSO4的混合液中加入1mol/L Ba(OH)2溶液,产生的沉淀与Ba(OH)2的体积的关系图正确的是 ( )
11.某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
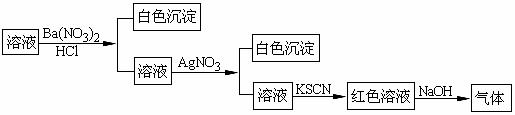
A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
10.将适量的SO2通过入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,继续滴入BsCl2溶液,产生白色沉淀。在上述一系列变化过程中,最终被还原的元素是 ( )
A.S B.Fe C.Cl D.N
9.已知碳酸钙的分解①CaCO3(s)==CaO(s)+CO2(g)仅在高温下自发:氯酸钾的分解②2KClO3(s)==2KCl(s)+3O2(g)在任何温度下都自发,下面有几组焓变数据,其中可能正确的是 ( )
A.△H1=-178.32kJ·mol-1 △H2=-78.3kJ·mol-1
B.△H1=+178.32kJ·mol-1 △H2=-78.3kJ·mol-1
C.△H1=-178.32kJ·mol-1 △H2=+78.3kJ·mol-1
D.△H1=+178.32kJ·mol-1 △H2=+78.3kJ·mol-1
8.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中,不正确的是 ( )
A.NH5中既有离子键又有共价键
B.NH5的熔沸点高于NH3
C.NH5固体投入少量水中,可产生两种气体
D.1mol NH5中含有5 mol N-H 键
7.下列各项操作中不发生先沉淀后溶解现象的是 ( )
①向饱和Na2CO3溶液中通入过量CO2
②向Fe(OH)3胶体中逐滴滴入过量的H2SO4
③向Ba(NO3)2溶液中通入过量SO2
④向石灰水中通入过量CO2
⑤向Na2SiO3溶液中滴入过量的盐酸
A.①②③ B.①②⑤ C.①②③⑤ D.①③⑤
6.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.常温常压下22.4L的CO2在一定条件下与足量的镁反应,转移4NA个电子
B.23g钠与一定量的氧气作用,若两者均无剩余,转移NA个电子
C.1mol/L(NH4)2SO4溶液中,含SO2-4NA个,NH+4少于2NA个
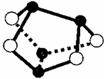
D.0.5mol雄黄(As4S4,结构如图)含有NA个S-S键
5.下列离子方程式正确的是 ( )
A.在KHSO4溶液中加入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO2-4=BaSO4↓+H2O
B.将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO2-3+2HClO
C.向碳酸氢钠溶液中滴入过量石灰水:HCO-3+Ca2++OH-=CaCO3↓+H2O
D.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO2-4恰好沉淀完全
2Al3++3SO2-4+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
4.下列指定溶液中,各组离子一定能大量共存的是 ( )
A.pH=1的溶液中:K+、Fe2+、Cl-、NO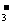
B.加入Al能放出H2的溶液中:NH+4、Cl-、SO2-4、HCO-3
C.在含有大量Fe3+的溶液中:NH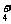 、Cl
、Cl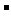 、Na+、SCN-
、Na+、SCN-
D.由水电离的c(OH-)=10-13 mol·L-1的溶液中:Ba2+、Cl-、Na+、Br-
3.应用元素周期律,判断下列语句,其中正确的组合是 ( )
①碱金属单质的熔点随原子序数的增大而降低
②砹(At)是第VIIA族,其氢化物的稳定大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(TI)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A.①③④ B.①③⑥ C.③④⑤ D.②④⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com