
8.已知反应:□AgF+□Cl2+□H2O==9AgCl+□AgClO3+□HF+1O2;下列说法正确的是 ( )
A.反应中的还原剂只有H2O
B.每生成9mol的AgCl时,消耗掉10mol的AgF
C.反应中的氧化剂是AgF
D.生成1molO2时,被还原的Cl2为5mol
7.下列各组离子中,在碱性溶液能大量共存,且在加入盐酸的过程中会产生气体和沉淀的是 ( )
A.Na+、NO-3、AlO-、SO2-4 B.Na+、NO-3、SiO2-3、K+
C.K+、Cl-、AlO-2、CO2-3 D.Na+、Cl-、HCO-3、Ca2+
6.俄罗斯杜布纳核研究所和美国劳伦斯利弗莫尔实验室的科学家在2004年2月的美国《物理论论C》杂志上发表文章宣布,他们新合成了元素周期表上的第115号和第113号元素。科学家在利用回旋加速器进行的实验中,用具有20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为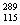 X。下列有关叙述正确的是 ( )
X。下列有关叙述正确的是 ( )
A.115号元素衰变成113号元素是化学变化
B.核素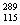 X中中子数与质子数之差为174
X中中子数与质子数之差为174
C.113号元素最高正价应为+3
D.115号与113号元素的原子质量比为115:113
29.(共10分)将3.2gCu溶于30mL amol/L过量的硝酸中,假设硝酸的还原产物只有NO和NO2,反应结束后,将所得溶液加水稀释至1000mL,测得c(NO-3)为0.2mol/L。求:
(1)稀释后溶液中氢离子的物质的量浓度为 。
(2)生成的气体中NO的物质的量为 ,NO2的物质的量为
(用含a的关系式表示)。
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:
2NO2+2NaOH=NaNO3+NaNO2+H2O; NO2+NO+2NaOH=2NaNO2+H2O
若生成的混合气体能被NaOH溶液完全吸收,则a的取值范围为 。
28.(共17分)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
C(s)+H2O(g) 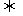 CO(g)+H2(g)ΔH=+131.3 kJ•mol-1,ΔS=+133.7J•(K•mol) -1
CO(g)+H2(g)ΔH=+131.3 kJ•mol-1,ΔS=+133.7J•(K•mol) -1
①该反应能否自发进行与 有关;
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母,下同)。
a.容器中的压强不变
b.1 mol H-H键断裂的同时断裂2 mol H-O键
c.v正(CO) = v逆(H2O)
d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) 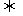 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
|
实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所 需时间/min |
||
|
H2O |
CO |
H2 |
CO |
|||
|
1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
|
2 |
900 |
1 |
2 |
0.4 |
1.6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
①实验1中以v(CO2) 表示的反应速率为 。
②该反应的逆反应为 (填“吸”或“放”)热反应
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是 (用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:
CO2(g)+3H2(g)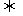 CH3OH(g)+H2O(g) ,下图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol
CO2和3mol H2,下列措施中能使c (CH3OH)增大的是________。
CH3OH(g)+H2O(g) ,下图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol
CO2和3mol H2,下列措施中能使c (CH3OH)增大的是________。
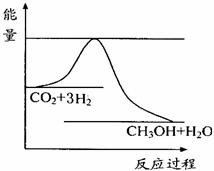
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1mol CO2和3mol H2
27.(共15分)有关元素X、Y、Z、D、E的信息如下
|
元素 |
有关信息 |
|
X |
元素主要化合价为-2,原子半径为0.074nm |
|
Y |
所在主族序数与所在周期序数之差为4 |
|
Z |
原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
|
D |
最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
|
E |
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为
。
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号) 。
①保存EY2溶液时,需向溶液加入少量E单质
②通常实验室配制EY3溶液时,直接用水溶解EY3固体
③EY2只能通过置换反应生成,EY3只能通过化合反应生成
④铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
⑤向淀粉碘化钾溶液和苯酚溶液中分别滴加几滴EY3的浓溶液,原无色溶液都变为紫色
(3)用化学符号表示D2Z的水溶液中各粒子的浓度关系,如 > > > > 。
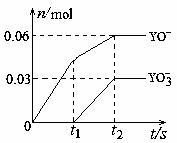
(4)将一定量的Y单质通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含Y元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。该苛性钾溶液中KOH的质量是 ,该反应中转移电子的物质的量是 。
26.(共8分)2009年3月底至4月中旬,墨西哥、美国等多国连接暴发甲型H1N1型流感 (或称H1N1型猪流感)疫情,防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感。
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式: 。
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了还原反应的是 。
A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2 → ClO2↑+ H+ +Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是 。
(3)有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为 。
25.某温度时,用惰性电极电解硝酸钠的不饱和溶液。若两极收集气体总体积为22.4aL时,剩余溶液恢复至原温,析出溶质mg;若两极收集到气体总体积为33.6aL时,剩余溶液恢复至原温,析出溶质ng。则硝酸钠在该温度时的溶解度是(气体体积均已折合为标准状况下的体积) ( )
A.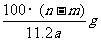 B.
B.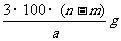
C.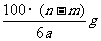 D.
D.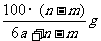
第Ⅱ卷(非选择题,共50分)
24.某无色溶液中可能含有I+、NH+4、Cu2+、SO2-3,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是 ( )
①肯定不含I-; ②肯定不含Cu2+
③肯定含有SO2-3 ④可能含有I-
⑤可能含有SO2-3
A.①②③ B.②④⑤ C.①②⑤ D.②③④
23.反应A2+B2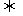 2AB在温度和压强改变条件下,产物AB的生成情况如图所示。A为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是 ( )
2AB在温度和压强改变条件下,产物AB的生成情况如图所示。A为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是 ( )
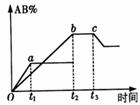
A.A2、B2、AB均为气体,正反应放热
B.AB为气体,A2、B2中最少有一种为非气体,正反应放热
C.AB为气体,A2、B2中最少有一种为非气体,正反应吸热
D.AB为固体,A2、B2中最少有一种为非气体,正反应吸热
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com