
21.(10分)有X、Y、Z三种常见的元素,已知:
①X2-、Y一均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色;
③X单质在空气中可燃烧生成一种无色有刺激性气味的气体。
请回答:
(1)Y的最高价氧化物对应水化物的化学式是 。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是 。
此液体具有的性质是 (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插人电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)①一定条件下,1 mol X单质在空气中燃烧生成的气体被O2氧化放出的热量为98.0 kJ。若2mol该气体与1mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为 。
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)溶液在一定条件下反应,可生成一种强酸和一种氧化物(一种新型自来水消毒剂),且有1.5×6.02×1023个电子转移,该反应的化学方程式是
。
20.(12分)A、B、C、D、E均为可溶于水的固体,组成它们的离子有如下表所示,分别取它们的水溶液进行实验,结果如下:(阴离子不能重复,阳离子可以重复)
|
阳离子 |
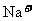 、 、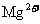 、 、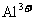 、 、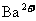 |
|
阴离子 |
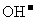 、 、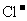 、 、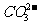 、 、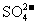 、 、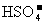 |
①A溶液与B溶液混合有白色沉淀及气体产生,且沉淀溶于E溶液;
②A溶液与c溶液混合有白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液混合有白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加人过量D溶液,沉淀量有所减少。
据此推断它们是:
Ⅰ.A ;B ;D 。
Ⅱ.请完成下列实验步骤的离子方程式:
(1)步骤①中生成白色沉淀的离子方程式
(2)步骤②中白色沉淀溶解的离子方程式
Ⅲ.为确定E中的阳离子还应进行的实验操作是 。
19.(12分)按下面所要求的化学用语,完成本题。
(1)铜元素原子的外围电子排布式: ;
(2)铬元素的简写电子排布式(用“原子实”表示内层): ;
(3)溴元素的原子结构示意图: ;
(4)NaHSO4溶液滴加到有酚酞试液的Ba(OH)4溶液中,当溶液的颜色刚好由红色变为无色时,反应的离子方程式为 ;
(5)向Ba(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,写出反应的离子方程式
;在上述溶液中继续滴入NaHSO4溶液,此时离子方程式为 ;
18.某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1,用石墨电极电解该混合液。下列叙述不正确的是 ( )
A.阴极自始至终均析出H2 B.阳极先析出Cl2,后析出O2
C.电解最后阶段为电解水 D.溶液pH不断增大,最后为7
第Ⅱ卷(非选择题共56分)
17.将一定量的Fe和Fe2O2的混合物投入250 mL、1.8mol/L的HNO3溶液中,当固体混合物完全溶解后,在标准状况下生成1.12L NO(HNO3的还原产物仅此一种),再向反应后的溶液中加入1.0mol/L NaOH溶液,若要使铁元素完全沉淀下来,所加入的NaOH溶液体积最少应为 ( )
A.300 mL B.400mL C.450mL D.500mL
16.已知下列分子或离子在酸性生条件下都能氧化KI,自身发生如下变化: ,
,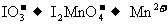 ,
,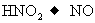 如果分别用这些物质氧化KI,得到相同量的I2,需要下列物质最少的是 ( )
如果分别用这些物质氧化KI,得到相同量的I2,需要下列物质最少的是 ( )
A.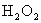 B.
B.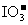 C.
C.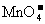 D.
D.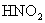
15.下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是
( )
A.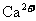 、
、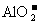 、
、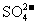 、
、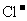 B.
B. 、
、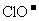 、
、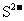 、
、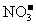
C.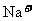 、
、 、
、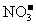 、
、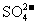 D.
D.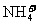 、
、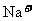 、
、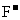 、
、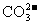
14.美国圣路易斯大学科学家在2004年研制出了一种新型的乙醇电池(DEFC),它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为: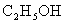

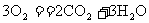 ,电池示意图如下。下列说法不正确的是 ( )
,电池示意图如下。下列说法不正确的是 ( )
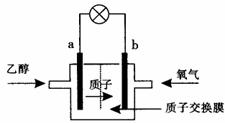
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.1mol乙醇被氧化产生6NAq库仑的电量(每个电子所带电量为q库仑,NA为阿佛加得罗常数
D.电池正极的电极反应为:4H++O2+4e-==2H2O
13.有两种短周期元素X和Y,可组成化合物XY3,当Y的原子序数为m时,X的原子序数为①m一4 ②m+4 ③m+8 ④m一2 ⑤m+6。其中正确的组合是 ( )
A.只有①②④ B.只有①②⑤ C.①②③⑤ D.①②③④⑤
12.有一稀硫酸和稀硝酸的混合酸,其中,H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L取10ml。此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体体积为(设反应中HNO3被还原成NO) ( )
A.0.672L B.0.448L
C.0.896L D.0.224L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com