
31.(8分)⑴工业上合成氨的反应方程式为_____________________,反应是在_______中进行,该设备的出口处的气体是____________(填写分子式)。
⑵纯水中含有10电子的粒子有_____种。
⑶向氢氧化钠溶液中逐渐加入盐酸至中性的过程中,水的电离程度______(填增大、减小、不变)。
⑷将1mol/L的氯化铁溶液和3mol/L的硫氰化钾溶液等体积混合,所得溶液中K+的物质的量浓度为______mol/L。
⑸用润湿的pH试纸测得的0.01mol/LNaOH溶液的pH_____12(填<、>、=)。
30.(4分)25℃时,有0.1 mol·L-1的下列溶液:①Na2SO4 ②NH4Cl ③H2SO4
④Ba(OH)2 ⑤NaOH ⑥Na2CO3 ⑦HCl。请按要求回答下列问题(填序号)
(1)溶液酸性最强的是_________。
(2)溶液碱性最强的是_________。
(3)溶液的pH值由大到小的排列次序是_______________________。
29.(14分)
(1)氯化铝水溶液呈 性 ,原因是(用离子方程式表示):______。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。实验室在配制AlCl3的溶液时,常将AlCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)相同物质的量浓度下的各溶液:NaX、NaY、NaZ,其PH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序为: ______;
(3)含有一定量(NH4)2SO4和NH3·H2O的水溶液称为“缓冲溶液”在此溶液中加入少量的强酸或者强碱时,溶液的pH几乎不变,这可由下列离子方程式来说明。
加酸时:NH3·H2O+H+=NH4++H2O 加碱时:NH4++OH-= NH3·H2O
由于(NH4)2SO4和NH3·H2O的大量存在,加少量酸或碱时,溶液中c(H+)与c(OH-)基本保持不变;含有一定量NaH2PO4和Na2HPO4的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或者强碱时发生的离子反应方程式:
加酸时: ;
加碱时: 。
28.两人用同一瓶标准盐酸滴定同一瓶NaOH溶液,甲将锥形瓶用NaOH待测液润洗后,使用水洗过的碱式滴定管取碱液于锥形瓶中,乙则用甲用过的碱式滴定管另取碱液于刚用水洗过且存有蒸馏水珠的锥形瓶中,其他操作及读数全部正确。下列说法正确的是( )
A.甲操作正确 B.乙操作有误
C.甲测定数值一定比乙小 D.乙实际测得值较准确
卷Ⅱ(非选择题,共44分)
27.在温度一定的条件下,对0.1mol/L的氨水稀释的过程中始终保持不变的是:( )
A.水电离产生的c(H+)与c(OH-)的积
B.n(NH+ 4)、n(NH 3)、n(NH3·H2O)的和
C.c(NH+ 4)与c(NH3·H2O)的比值
D.溶液中c(H+)与c(OH-)的和
26.选取两个密闭容器A、B,向A、B中都加入SO2和O2各l g,发生反应2SO2(g)+ O2(g)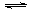 2SO3(g),正反应放热。反应开始之前A与B同温、同压、同容,反应开始之后A保持恒温、恒容,B保持恒温、恒压,并都达到平衡状态。下列说法中,正确的是 ( )
2SO3(g),正反应放热。反应开始之前A与B同温、同压、同容,反应开始之后A保持恒温、恒容,B保持恒温、恒压,并都达到平衡状态。下列说法中,正确的是 ( )
A.平衡时SO2的转化率:A > B
B.平衡时的化学反应速率:A > B
C.平衡时混合气体的总物质的量:A < B
D.可逆反应从开始到平衡放出的热量:A < B
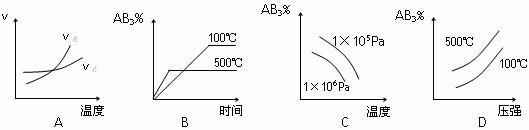
25.对于可逆反应2AB3(g) A2(g)+3B2(g),正反应吸热,下列图像正确的是( )
A2(g)+3B2(g),正反应吸热,下列图像正确的是( )
24.若NA表示阿伏加德罗常数,则下列说法正确的是 ( )
A.100℃时水的Kw=1×10-12,此时水电离产生的H+和OH-个数之和为2×10-6NA
B.1L0.1mol/L的盐酸中含有的HCl分子数为0.1 NA
C.1L pH=1的H2SO4溶液中含有的SO2- 4为0.05 NA
D.1molN2和3molH2在有催化剂加热的条件下充分反应生成2 NA个NH3
23.下图为某化学反应的速率与时间的关系示意图。下列有关t1时刻改变条件的说法正确的是( )

A.2SO2(g)+O2(g)  2SO3(g),正反应放热,t1时刻升高温度
2SO3(g),正反应放热,t1时刻升高温度
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g),正反应放热,t1时刻增大O2浓度
4NO(g)+6H2O(g),正反应放热,t1时刻增大O2浓度
C.H2O(g)+CO(g)  H2(g)+CO2(g),正反应吸热,t1时刻增大压强
H2(g)+CO2(g),正反应吸热,t1时刻增大压强
D.C(s)+H2O(g)  CO(g)+H2(g),正反应吸热,t1时刻升高温度
CO(g)+H2(g),正反应吸热,t1时刻升高温度
22.下列溶液中有关微粒的物质的量浓度关系正确的是 ( )
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):
c(Na+)=c(HRO- 3)+2c(RO2- 3)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:
c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③NH4HSO4三种溶液中c(NH+ 4):①>②>③
D.相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com