
12.设NA为阿伏加德罗常数。下列说法正确的是 ( )
A.58.5克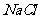 晶体中离子总数为
晶体中离子总数为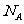 个
个
B.常温常压下,34克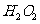 中含有共用电子对数为3
中含有共用电子对数为3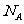
C.常温常压下,1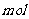 羟基(-OH)所含电子数为10
羟基(-OH)所含电子数为10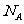
D.1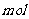
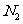 和
和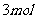
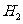 在一定条件下反应时转移的电子数为
在一定条件下反应时转移的电子数为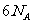
11.下列说法正确的是 ( )
A.金属锂在足量O2中点燃生成Li2O2
B.HF、HCl、HBr、HI的稳定性和水溶液酸性都依次增强
C.16O2、18O3互为同位素
D.硝酸溶液浓度越大氧化性越强
10.工业制硫酸中,从接触室出来的气体缓慢通入到BaCl2溶液中,则 ( )
A.析出BaSO3沉淀 B.析出BaSO4沉淀
C.不析出任何沉淀 D.析出BaSO3和BaSO4沉淀
9.下列离子方程式中正确的是 ( )
A.同浓度同体积的明矾与Ba(OH)2溶液反应:
3Ba2++6OH-+2Al3++3SO42-= 3BaSO4↓+2Al(OH)3↓
B.硫氢化铵溶液与过量烧碱溶液反应:NH4++OH-=NH3↑+H2O
C.苯酚钠溶液中通入少量CO2: -O-+CO2+H2O→
-O-+CO2+H2O→ -OH+CO32-
-OH+CO32-
D.FeBr2溶液中通入足量氯水:2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl-
8.实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是 ( )
A.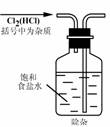 B.
B.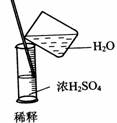
C. D.
D.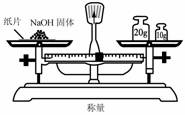
7.某溶液中含有CH3COO-、I-、SO32-、HCO3-、CO32-等五种离子。将过量的Na2O2固体加入其中后,仍能大量存在的离子是 ( )
A.CH3COO-、I-、CO32- B.I-、SO32-、CO32-
C.SO32-、HCO3- D.CH3COO-、CO32-
6.环境问题是人们越来越关注的问题,下列有关说法正确的是 ( )
A.pH为5.6的降水称为酸雨
B.CO、CH4造成了光化学烟雾
C.煤燃烧时加入适量的大理石可减少废气中SO2的量
D.海水中的藻类疯狂的生长所引发的赤潮是因为海水中有大量的氮肥
35.(11分)为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。试填空。
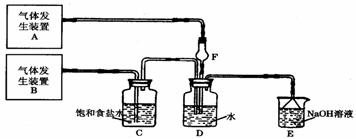
(1)D装置中主要反应的离子方程式为 ,F仪器的作用是: 。
(2)为验证通入D装置中气体是Cl2还是SO2过量,兴趣小组的同学准备了以下试剂:
a 氯化铁稀溶液 b 氯化亚铁溶液 c硫氰化钾溶液
d 苯酚溶液 d 品红溶液 f 酸性高锰酸钾溶液
①若Cl2过量:取适量D中溶液滴加至盛有 (选填一个符号)试剂的试管内,再加入 (选填一个符号)试剂,发生的现象是: ;
②若选用上述试剂中的一种结合必要的操作就可以验证通入C装置中气体是Cl2过量还是SO2过量,该试剂是_________。(选填一个符号)
必要操作和结论______________________________ ________。
34.(14分)(Ⅰ)A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体。E、F、G、H、I为五种化合物,F不溶水,E为气体且极易溶水成为无色溶液,G溶水得黄棕色溶液。这九种物质间反应的转化关系如图所示。
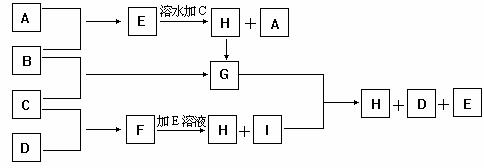
(1)写出四种单质的化学式
A________ B_________ C_________ D________
(2)写出E+F→H+I的离子方程式
(3)写出G+I→H+D+E的化学方程式
(4)某工厂用B制漂白粉。
①写出制漂白粉的化学方程式 。
②为测定该工厂制得的漂白粉中有效成分的含量,某该小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配置成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸(此时发生的离子方程式为: ),静置。待完全反应后,用0.1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为 (保留到小数点后两位)。
33.(10分)在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g) 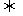 pC(g)。
pC(g)。
(1)欲使A与B的转化率等于m:n ,则起始加入A、B的物质的量之比为 .
(2)充入一定量的A、B,若在不同条件下C的体积分数随时间的变化如图1-1所示,则:
m+n p(填“>”、“<”或“=”),
T1 T2填(“>”、“<”或“=”),
该反应的△H 0(“>”、“<”或“=”)。
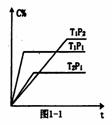
(3)一定条件下,从正反应开始达到化学平衡过程中,混和气体的平均相对分子质量随时间的变化如图1-2所示。若在恒温恒容的条件下,向原平衡体系中再通入一定量的C,则体系中气体的平均相对分子质量将 (填“增大”、“减小”、“不变”或“无法确定”)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com