
2、食品卫生与身体健康密切相关,下列做法对人体无害的是
A.香肠中加过量亚硝酸钠以保持肉类新鲜
B.用“瘦肉精”(一种含激素的饲料) 喂饲生猪
C.用小苏打做发酵粉做面包
D.用福尔马林保鲜鱼肉等食品
1、化学与科学发展、生产、生活密切相关。下列有关说法中正确的是
A.红外光谱(IR)是利用化学原理确定有机物官能团的科学方法
B.将煤气化为CO和氢气等燃料有利于提高煤的利用率
C.卫生部公布的首批非法食品添加剂中的三聚氰胺是一种含氮量很高的蛋白质
D.聚乙烯和聚氯乙烯塑料薄膜均可通过加聚反应得到,所以聚乙烯、聚氯乙烯塑料袋均用来包装油性食品
2、可能用到的相对原子质量: H-l O-16 C-12
Ⅰ卷:选择题(每小题只有一个正确选项,每小题2分,共40分)
29.八角茴香属于草本植物,是我国民间常用做烹调的香料。医学研究成果显示,从八角茴香中可以提取到莽草酸,莽草酸有抗炎、镇痛作用,是合成某些抗癌药物的中间体,还是合成“达菲”的前体。莽草酸的结构简式和分子结构模型如下图所示。
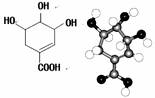
在有机物分子中,若碳原子连接四个不同的原子或原子团,该碳原子称为不对称碳原子(或手性碳原子)。具有手性碳原子的有机物具有光学活性。
请回答下列问题:
(1)莽草酸分子式是____________,莽草酸分子中含有的官能团是______________。
(2)一定量的莽草酸与足量Na、 NaHCO3(溶液)反应时消耗两者的物质的量之比为____________,当莽草酸与乙酸以物质的量之比1:1发生酯化反应可生成___________种不同结构的酯
(3)莽草酸跟有机物A在一定条件发生酯化反应可生成一种相对分子质量为202的酯类物质。写出2种A可能的结构简式_____________________________________。
(4)已知莽草酸中有3个手性碳原子,若发生反应:

则使莽草酸分子转化成只具有2个手性碳原子的物质,请再设计一种方法,通过一步反应也使莽草酸分子转化成只具有2个手性碳原子的物质,有关化学方程式为
_ __________________________________________________。
28.某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图装置进行有关实验,请回答:
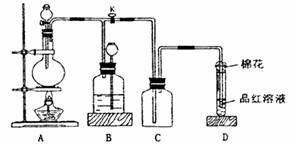
(1)装置D中试管口放置的棉花中应浸一种液体,这种液体的作用是 。
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是 。 B中应放置的液体是(填字母) 。
a.NaOH溶液
b.酸性KMnO4 溶液
c.浓溴水
d.饱和NaHSO3溶液
(3)铜不能与稀硫酸直接反应得到硫酸铜,但可用下面方法制取:将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶可制得硫酸铜晶体(装置如图1、2所示)。
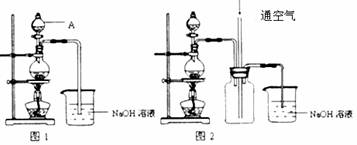
①把浓硝酸分多次加入到铜粉与稀硫酸的混合物中的目的是_________________。
②已知NO不能被NaOH溶液直接吸收,但已知有如下两个反应:
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO3+NaNO2+H2O。图2是图1的改进装置,其优点除可以防止倒吸外还有:_______________________。
③如果用1molCu来制取1molCuSO4,则所需浓硝酸中HNO3的质量为________,(假设HNO3的还原产物全为NO),若所得尾气恰好被NaOH溶液吸收为NaNO2,需通入空气的体积为_____(假设实验体积为标准状况下测定,保留小数点后一位,并忽略装置中原有空气的影响)
27.已知A-F是中学化学中常见物质,其中C、E为短周期元素的气体单质,B为无色为液体,B分子中有18个电子。D为常见三大强酸之一,其浓溶液有吸水性和脱水性,F的浓溶液与X共热通常用于实验室制备C,X是一种黑色粉末。反应中部分生成物已略去。
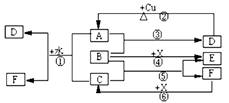
试回答下列问题:
(1)根据图中信息, C. X氧化性从强到弱的顺序是(直接用C、X表示) 。
(2)写出D和X的化学式D X ;
(3)写出反应②. ⑤的化学方程式:
②
⑤
(4)写出反应①、 ⑥的离子方程式
①_________________________________________________;
⑥_________________________________________________
26.A、 B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中常温下有两种是气体,两种是固体。
(1)写出由B、 C二元素所形成的原子个数比为1∶1的化合物的电子式__________,其晶体中存在的化学键有____________________(填化学键名称)。
(2)写出均由A、 B、C、D四种元素组成的两种化合物的水溶液发生反应的离子方程式为_____________。
写出金属铝与A、 B、 C三种元素组成的化合物的水溶液发生反应的离子方程式_____________。
(3)用A元素的单质与B元素的单质可制成新型的化学电源,已在宇宙飞船中使用。其构造如下图所示。两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。则a是___极,电极反应式为________ 。
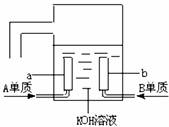
13.如图所示,⑴编号1-6代表六种物质,它们分别是:A,石灰水;B,铁;C,硝酸银溶液;D,碳酸钾溶液;E,盐酸;F,氯化铝溶液;⑵凡连线两端方框内的物质都能相互发生反应。试根据图中关系,确定方框内物质按序号1-6依次为(用代码A-F表示)
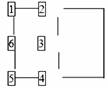
A.FDAEBC B.BCAEFD
C.ACBDFE D.DFEABC
 非选择题部分
非选择题部分
12.下列制备反应中不可能在工业中实现的是: ( )
A.用钠和氯化钾反应置换出钾
B.用电解氯化镁溶液的方法制备金属镁
C.用乙醇和氢氧化钠反应来制备乙醇钠
D.由苯和丙烯反应制取异丙苯
11.下列离子方程式正确的是 ( )
A.碳酸氢钠溶液与少量澄清石灰水反应: HCO3-+Ca2++OH-=CaCO3↓+H2O
B.用惰性电极电解饱和氯化镁溶液: 2Cl-+2H2O=2OH-+H2↑+Cl2↑
C.向硫酸铝溶液中滴加过量的氨水溶液: Al3++4NH3·H2O =AlO2-+4NH4++2H2O
D.用碳酸钠溶液吸收少量二氧化硫气体: 2CO32-+SO2+H2O=2HCO3-+SO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com