
6.下列离子方程式正确的是 ( )
A.在硫酸铜溶液中加入过量氢氧化钡溶液:Ba2++SO42-=BaSO4↓
B.碳酸氢钠溶液与少量石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
C.向氯化铝溶液中加入过量氨水:A13++4NH3·H2O =A1O2-+4NH4++2H2O
D.NH4HCO3溶液与过量NaOH溶液混合后加热:NH4++OH-=NH3↑+H2O
5.下列各项中表达正确的是 ( )
A.F原子结构示意图: B.次氯酸电子式
B.次氯酸电子式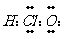
C.H、D、T表示同一种核素 D.CH4分子的球棍模型: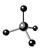
4.下列操作或仪器的选用正确的是 ( )
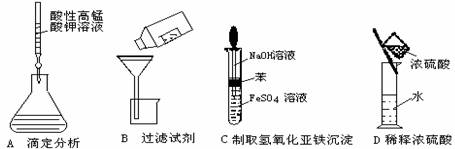
3.2008年北京奥运会开幕式的焰火:“脚印”、“笑脸”、“五环”,给世界各国留下深刻印象。其主要原料是黑火药,还有草酸钠、碳酸铜(发出绿色的光)等发色剂和氯酸钾、镁铝金属粉末等添加剂。据此判断下列说法正确的是 ( )
A.碳酸铜因为受热分解才发出绿色的光
B.氯酸钾的主要用途是产生紫色的焰火
C.焰火的产生与原子核外电子发生跃迁释放能量有关
D.黑火药的主要成分是木炭、硫磺
1.清蒸大闸蟹由青色变成红色,一同学认为这种红色物质可能像酸碱指示剂一样,遇到酸或碱颜色会发生改变。就这位同学的看法而言,这应该属于科学探究中的 ( )
A.实验 B.假设 C.观察 D.分类
2.生物学家借助新的显微技术,成功观察到小于200纳米的微粒。下列分散系中,分散质微粒半径最小的是 ( )
A.雾 B.蛋白质溶液 C.石灰乳 D.KNO3溶液
21、(12分)将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
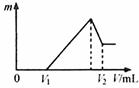
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。
当V1=160mL时,则金属粉末中n(Mg)= mol, V2= mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积
V(NaOH)= mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是: 。
20、(14分)在半导体工业中,有一道工序叫烧氢。烧氢的工艺流程如图所示。工作时,是将石英管D出口处氢气点燃。半导体硅片、焊片和金属零件从石英管口送入加热区,在氢气还原气氛中加热使焊片熔化,将单晶硅与金属零件焊接在一起。焊接后再将零件拉至冷却区,冷却后取出。烧氢工艺中的氢气纯度要求极高,工业氢气虽含氢量达99.9%,但仍含有极微量的水蒸气和氧气,所以点燃氢气前应检验氢气的纯度。试回答下列问题。
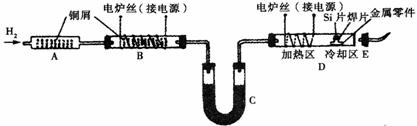
(1)装置B的作用是_____ ______;
B中发生反应的化学方程式是__________ ___,______ ________。
(2)装置C中的物质是______ ______;C的作用是____________ ___________。
(3)点燃氢气前将E(带导管胶塞)接在D的出口处,目的是____ _________。
(4)装置A是安全瓶,可以防止氢气燃烧回火,引起爆炸,其中填充大量纯铜屑的作用是______________________________ 。
19、(14分)小冬同学在家务劳动时跟爸爸学习杀鱼,在杀鱼时对从鱼腹内取出的鱼鳔产生了兴趣。他拟定“探究鱼鳔内气体的成分和体积”作为课题进行研究。小冬查阅资料获知:这种鱼的鱼鳔内氧气占四分之一,其余气体是二氧化碳和氮气。
他设计了如下实验方案:
Ⅰ.测量鳔内气体的体积。小冬设计了两种方法:
(1)用医用注射器(带有准确的刻度)抽取鱼鳔内的气体,测量其体积;
(2)在水槽中倒扣一个盛满水的量筒,用镊子夹住鱼鳔,将鱼鳔尖端放在量筒口处,用一根针在水下刺破鱼鳔尖端,用排水集气法收集鳔内的气体并测量其体积。
你认为其中测量结果不准确的是 ,理由是
Ⅱ.探究鳔内气体的成分。小冬收集了鳔内气体分别装在集气瓶和医用注射器中进行如下实验。
|
实验编号 |
实验记录 |
|
|
(3)验证鳔内含有氧气 |
将燃着的木条放入集气瓶中 |
木条能继续燃烧,证明含有氧气 |
|
(4)验证鳔内含二氧化碳 |
操作方法:
|
实验现象:
该反应的离子方程式是: 该实验中能否使用上述(3)实验结束后集气瓶中剩余的气体,为什么? 。 |
|
(5)分离出氮气 |
取一份装在100mL医用注射器中的鳔内气体进行分离:第一步,将气体通过 (填试剂)除去氧气;第二步,将剩余气体通过足量的
除去二氧化碳;第三步,将剩余气体通 过 进行干燥,即可得纯净的氮气。 |
第三步实验时还可以选用 作干燥剂。 |
18、(15分)为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
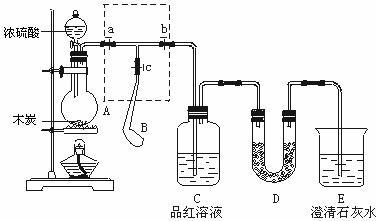
请回答下列问题:
(1)实验前欲检查装置A的气密性,可以采取的操作是 ;
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是 (用操作编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)实验时,装置C中的现象为_________ ;
(4)当D中产生__________(多选不得分)现象时,可以说明使E中澄清石灰水变浑的是CO2,而不是SO2;
A.进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变
B.脱脂棉上蓝色均变浅
C.脱脂棉上蓝色褪去
则装置D的作用为 。
17、(9分)如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同。试回答
(1)此实验中,观察到的现象有:
① , ② 。
(2)写出实验过程中反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com