
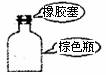
8.下列选用的相关仪器符合实验要求的是
|
A |
B |
C |
D |
|
存放浓硝酸 |
分离水和乙酸乙酯 |
准确量取9.50mL水 |
实验室制乙烯 |
 |
 |
 |
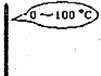 |
7.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是 ( )
A.由mXa+与NYb-得,m+a=n – b
B.X2-的还原性一定大于Y-
C.X、Y一定不是同周期元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
6.用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.在1L 0.1mol·L-1碳酸钠溶液中,阴离子总数大于0.1NA
B.标准状况下,5.6L一氧化氮和5.6L氧气混合后的分子总数为0.5NA
C.58.5g的氯化钠固体中含有NA个氯化钠分子
D.1mol乙烷分子含有8NA个共价键
5.在pH=13的无色溶液中,可以大量共存的离子组是 ( )
A.NH+4、NO-3、K+、SO2-4 B.CO2-3、NO-3、HCO-3、Na+
C.Na+、ClO-、AlO-2、NO-3 D.Fe3+、K+、Na+、SO2-4
4.下列关于溶液和胶体的叙述正确的是 ( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明亮的光路,前者则没有
3.下列关于氢键的说法正确的是 ( )
A.每一个水分子内含有两个氢键
B.冰、水中都存在氢键
C.分子间形成的氢键与物质的熔点和沸点无关
D.H2O是一种非常稳定的化合物,这是由于氢键所致
2.据2009年4月6日搜狐网站报道:国家质检总局称,在我国销售的德国NUK牌婴儿爽身粉含有一级致癌物“滑石粉”。已知滑石粉的化学式为Mg3(Si4O10)(OH)12,色白、滑爽、柔软、耐火。下列有关说法不正确的是 ( )
A.滑石粉属于无机硅酸盐类物质
B.滑石粉组成可表示为3MgO·4SiO2·H2O
C.爽身粉中添加滑石粉是利用它的滑爽、柔软、耐火性
D.滑石粉可能会与氢氟酸、NaOH溶液发生反应
1.下列化合物不能通过化合反应获得的是 ( )
A.Na2O2 B.Al2S3 C.CuS D.Fe(OH)3
27.(10分)平达喜是常用的中和胃酸的药物,它的化学成分是铝和镁的碱式碳酸盐,取该碱式盐3.01g,逐滴加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全。若在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g。
问:(1)固体中CO32-的物质的量是
(2)固体中OH-的物质的量是
(3)固体中Al3+的物质的量是
(4)固体中氢元素的质量分数为0.040,试通过计算推测该碱式盐的化学式。
26.(10分)铁钉镀锌
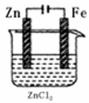
(1)该实验为无氰镀锌法,以烧杯作为电解槽,锌片作阳极,镀件铁钉作阴极。阳极反应式 ,阴极反应式 。
(2)实验仪器:托盘天平,烧杯,玻璃棒,药匙,导线,细纱纸,直流电源,酒精灯,pH试纸
(3)实验试剂:铁钉,锌片,2mol/LNaOH溶液,固体KCl,固体ZnCl2,浓HCl,浓硝酸,蒸馏水
(4)电解液的配制:先向烧杯中加入50ml蒸馏水,再加入3.5g ZnCl2,12.5gKCl,搅拌使之溶解你认为KCl的作用可能为 ,用硼酸或盐酸调节溶液的pH为5-6。pH太高会 ,pH太低会 。镀前处理大致包括以下基本内容:除油、除锈、除氧化层、浸蚀、酸洗、活化等。
(5)镀件的处理:用细砂纸打磨铁钉,使铁钉粗糙的表面变得光滑,用水洗净;把铁钉放入到80℃ 2mol/L NaOH溶液中浸泡5分钟,除去油污,用水洗净;再将铁钉放入45℃的浓盐酸中浸泡2分钟,取出,洗净;最后将铁钉放入V(浓硝酸):V(水)=1:100的稀硝酸中浸泡3-5秒,取出,洗净。你认为把镀件放入稀硝酸的作用是 。
(6)电镀操作:用烧杯做电解槽,锌片作阳极,镀件铁钉作阴极,接通6V的支流电源,电解25分钟。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com