
17.为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g样品加热,其质量变为w2g,则该样品的纯度(质量分数)是 ( )
A.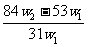 B.
B.
C.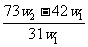 D.
D.
16.已知一定温度下,X(g)+2Y(g) 2Z(g);△H=-aJ/mol(a>0)。现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达到平衡时,放出热量bkJ;向密闭容器乙中通入2molX和2molY,达平衡状态时,放出热量ckJ,则下列关系正确的是 ( )
2Z(g);△H=-aJ/mol(a>0)。现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达到平衡时,放出热量bkJ;向密闭容器乙中通入2molX和2molY,达平衡状态时,放出热量ckJ,则下列关系正确的是 ( )
A.a=b B.c>2a C.c>2b D.c=2a
15.按下图所示装置进行实验(其中C1、C2均是石墨电极),下列说法中正确的是( )
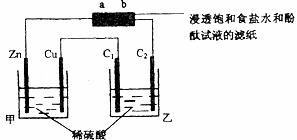
A.在标准状况下,锌极减轻3.25g时,Cu极上放出气体体积约为2.24L
B.发现b点附近显红色
C.在C1、C2电极所产生气体的体积比为2:1
D.乙池溶液的pH减小
14.标准状况下,aL CO2气体通过足量Na2O2,所得气体与bL NO混合时,可得cL气体,以下表达式不正确的是 ( )
A.若a = b,则 B.若a > b,则
B.若a > b,则
C.若a < b,则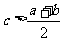 D.若a < b,则
D.若a < b,则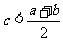
13.二氧化硫的催化氧化是放热反应。下列关于接触法制硫酸的叙述正确的是 ( )
A.为防止催化剂中毒,炉气在进入接触室之前需要净化
B.为了提高SO2的转化率,接触室内的反应温度选定在400℃-500℃
C.为了防止污染大气,从吸收塔出来的尾气常用NaOH溶液吸收
D.为了提高SO2的吸收效率,用稀硫酸代替水吸收SO3
12.下列离子方程式正确的是 ( )
A.向次氯酸钙浓溶液中通入过量的二氧化硫:Ca2++ClO-+SO2+H2O=CaSO4↓+Cl-+2H+
B.氧化铁粉末投入氢碘酸溶液中:Fe2O3+2HI+4H+=2Fe2++I2+3H2O
C.醋酸钡溶液和硫酸反应:Ba2++SO2-4=BaSO4↓
D.用惰性电极电解硝酸银溶液:4Ag++2H2O 4Ag+O2↑+4H+
4Ag+O2↑+4H+
11.9.2g金属钠投入到足量的重水中,则产生的气体中含有 ( )
A.0.2mol中子 B.0.4mol电子 C.0.2mol质子 D.0.4mol分子
10.下列各组物质相互混合反应,既有气体生成,最终又一定有沉淀生成的是 ( )
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中
A.①②③ B.②③④ C.①②④ D.①③④
9.下列有关热化学方程式的叙述正确的是 ( )
A.已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定
B.若含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:
NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l);△H=57.4kJ·mol-1
C.已知2C(s)+2O2(g)=2CO2(g);△H1;2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2
D.已知2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ·mol-1,则氢气的燃烧热为285.8kJ·mol-1
8.将下列各组离子混合于同一溶液中,不一定能得到沉淀的是 ( )
A.Ca2+、HCO-3、Na+、OH- B.Na+、AlO-2、H+、Cl-
C.Fe3+、Na+、Cl-、ClO- D.S2-、K+、SO2-2、H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com