
4、下列实验能达到预期目的的是( )
A.煮沸的1mol·L-1 NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体
B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱
C.称取19.0g SnCl2,用100mL蒸馏水溶解,配制1.0 molL-1 SnCl2溶液
D.测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱
3、下列说法正确的是( )
A.两难溶电解质作比较时,Ksp小的,溶解度一定小;
B. Ksp的大小取决于难溶电解质的量,所以离子浓度改变时,沉淀平衡会发生移动;
C.所谓沉淀完全就是用沉淀剂将溶液中某一离子除净;
D.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液
2、下列有关物质保存的说法正确的组合是( )
①钠应该密封在煤油中保存; ②过氧化钠可以露置在空气中保存;
③氯水应该密封在无色试剂瓶中保存; ④漂白粉不能露置在空气中保存。
A.①③ B.①②③④ C.①③④ D.①④
1、下列说法中,不正确的是( )
A.21世纪,化学科学还将继续推动材料科学的发展,使各种新型功能材料的生产成为可能
B.化学家可以在微观层面上操纵分子和原子,组装分子材料、分子器件和分子机器
C.放射性元素的发现和现代量子化学理论的建立,都是进入20世纪后现代化学的重大成就
D.化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中
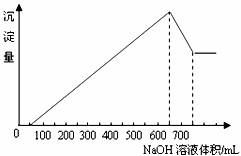
29.(8分)将等物质的量的两种金属氧化物完全溶解在100 mL某浓度的硫酸中,而后向其中逐滴加入l.00 mol/L的NaOH溶液。产生沉淀的量与加入NaOH的体积关系如下图。则:
⑴最初加入的50 mL NaOH溶液的作用是什么?
⑵计算所用硫酸的物质的量浓度。
⑶试判断两种氧化物可能是什么,并求其物质的量。
28.(12分)小章同学准备在实验室用下图所示装置模拟工业炼铁。请你据此回答下列问题:
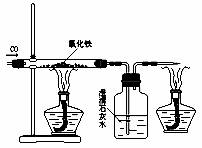
(1)实验中产生的现象主要有哪两点: 、 。
(2)实验中两个酒精灯的作用各是什么?左边: ;右边: 。
(3)当Fe2O3反应完全后,应先熄灭 (选填“左边”或“右边”)酒精灯。
(4)某同学实验完成后,发现过量的澄清石灰水增重0.44g,则该同学通入装置的CO气体质量 (选填“大于”、“等于”或“小于”)0.28g。
27.(14分)下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物。试推断:
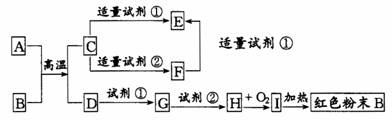
(1)写出物质的化学式:
A:________ C:________ Ⅰ:________
(2)写出下列反应的方程式:
C→F的离子方程式
A+B→C+D的化学方程式
F→E的离子方程式
H→I的化学方程式
26.(16分)(1)铁在氯气中燃烧的生成物溶于水制成饱和溶液,做如下实验:
(a)加入NaOH溶液,现象 离子方程式
(b)加入铁屑,现象 离子方程式
(c)滴入KSCN溶液,现象 离子方程式
(2)(a)一块表面有氧化膜的铝在氢氧化钠溶液中溶解的离子方程式_______________。
(b)偏铝酸钠溶液中通入少量二氧化碳,现象________________,离子方程式 。
25.向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(S、T、P)的气体。所得溶液中加入KSCN溶液无血红色出现,混合物中铁元素的质量分数为
A、68.6% B、77.8% C、81.4% D、无法计算
24.若在加入铝粉能放出氢气的溶液,分别加入下列各组离子,可能大量共存的是
A、NH4+ NO3- CO32- Na+ B、Na+ Ba2+ Mg2+ HCO3-
C、NO3- Ca2+ K+ Cl- D、NO3- K+ AlO2- OH-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com