
4.下列含有共价键的离子化合物是 ( )
A. 氯化镁 B. 溴化氢 C. 氧化钙 D. 氯化铵
3.我国的嫦娥探月工程已正式启动,据科学家预测月球的土壤中吸附着数百万吨的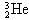 ,
,
而在地球上氦元素主要以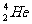 的形式存在,下列说法中正确的是
( )
的形式存在,下列说法中正确的是
( )
A.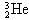 和
和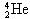 互为同位素
互为同位素
B.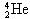 比
比 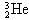 多一个质子
多一个质子
C.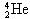 原子核内有4个中子
原子核内有4个中子
D.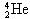 最外层电子数为2,所以
最外层电子数为2,所以  有较强的金属性
有较强的金属性
2.下列各项表达式正确的是 ( )
A.F-的结构示意图: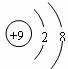
B.乙炔的分子模型示意图:
C.硫离子的核外电子排布式:1s22s22p63s23p4
D.氮分子的结构式: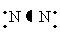
1.下列一些媒体中出现的说法,你认为科学的是 ( )
A.本饮料纯属天然,绝对不含化学物质
B.新粉刷过石灰浆的房间释放出CO2,严禁入内
C.水是取之不尽用之不竭的
D.易燃易爆的车间严禁穿化纤类衣服
20、(15 分)如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
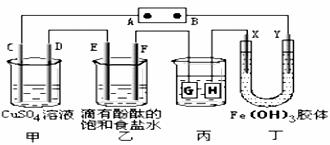
请回答:
(1)B极是电源的 极,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 在电场作用下向Y极移动。
(2)电解一段时间内甲、乙装置中的C、D、E、F电极均分别只有一种单质生成时,对应单质的物质的量之比为 ,乙中发生反应的离子方程式为 ,若要使电解后的甲装置中的溶液恢复到原浓度则需加入一定量的 。(填物质的化学式)
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”)。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 ,甲中溶液的pH (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是 。
19、(1)(3分)下列反应在210℃达到平衡:
PCl5(气)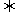 PCl3(气)+Cl2(气);
△H >0 K=1
①
PCl3(气)+Cl2(气);
△H >0 K=1
①
CO(气)+Cl2(气)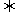 COCl2(气);△H<0 K=5×104 ②
COCl2(气);△H<0 K=5×104 ②
COCl2(气)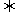 CO(气)+ Cl2(气);△H
>0 ③
CO(气)+ Cl2(气);△H
>0 ③
(1)反应②和反应③的K值表达式 (填“相同”或“不同”)
(2)降低Cl2浓度,反应③的K值 (填“增大”、“减少”或“不变”)
(3)要使反应①和反应②的K值相等,应采取的措施是
(a)反应①、反应②同时升高温度
(b)反应①、反应②同时降低温度
(c)反应①降低温度, 反应②维持210℃
(2)(10分)现将水蒸汽和CO气体分别通入到体积为1L的恒容密闭容器中进行反应。
H2O(g)+CO(g)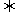 CO2(g)+H2(g);△H。得到以下三组数据,据此回答下列问题:
CO2(g)+H2(g);△H。得到以下三组数据,据此回答下列问题:
|
实验组 |
温度 |
起始量 |
平衡量 |
达到平衡所需时间 |
||
|
H2O |
CO |
H2 |
CO2 |
|||
|
1 |
650℃ |
1mol |
2mol |
0.8mol |
0.8mol |
5min |
|
2 |
900℃ |
0.5mol |
1mol |
0.2mol |
0.2mol |
3min |
|
3 |
900℃ |
a mol |
b mol |
c mol |
d mol |
t |
(1)由以上数据,实验1中以v(CO2)表示的反应速率为 mol·L-1·min-1。
(2)比较该反应实验1和实验2中CO的转化率: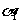
 ;该反应的反应热△H
;该反应的反应热△H
0。(两空填“>”、“=”或“<”)
(3)若实验3要达到与实验2等效的平衡状态,且t<3 min,则a、b应满足的关系是 ,实验3条件时反应的平衡常数为 。
(4)900℃时,若要重新达到平衡,使c(CO2)/c(CO)比值变小,在其他条件不变时,可采取的措施有(填字母) 。
A.使用高效催化剂 B.增大H2浓度 C.升高温度 D.缩小容器体积
18、(1)(2分)下图为常见仪器的部分结构(有的仪器被放大)

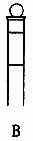


A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,则所使用的仪器是____ (填字母标号)。
(2)(9分)在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[Mr(Na2C2O4)=134.0],对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为:5C2O42-+2MnO4-+16H+→10CO2↑+2Mn2++8H2O以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol·L-1的高锰酸钾溶液500 mL。
步骤二:准确称取Na2C2O4固体m g放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70-80℃,用步骤一所配高锰酸钾溶液进行滴定。记录相关数据。
步骤三: 。
步骤四:计算得高锰酸钾的物质的量浓度。试回答下列问题:
①该滴定实验 (“需要”或“不需要”)加指示剂。
②步骤二中滴定操作图示正确的是__________(填编号)。
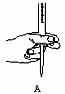

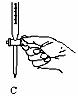
③步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色明显变快的原因可能是_________ ,最后又变慢的原因是 。
④请写出步骤三的操作内容 。
⑤若m的平均数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为 mol·L-1。
17、⑴(2分)298K、100kPa时,C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5kJ·mol-1 2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1 ,
请写出298K时由C(s,石墨)和H2(g)生成1molC2H2(g)的热化学方程式
(2)(3分)水是生命之源,也是化学反应中的主角。试回答下列问题: A、B、C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A、B、C与水反应的化学方程式:
;
(3)(2分)写出硫化钠在水溶液中水解的离子方程式 在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
(4)(4分)明矾可做净水剂是因为 ,有关的离子方程式为 ;向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是 ,有关的离子方程式 。
(5)(2分)下列哪些事实能说明醋酸是弱酸
①醋酸不易腐蚀衣服
②0.1mol/L的CH3COONa溶液的pH约为9。
③进行中和滴定时,等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多。
④0.1mol/L的CH3COOH溶液pH约为2.9。
⑤相同体积的pH均等于4的盐酸和CH3COOH溶液,被同一物质的量浓度的NaOH溶液中和,CH3COOH溶液消耗的NaOH溶液多。
⑥镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠可以降低反应速率但不改变产生气体的总量。
16、下列离子方程式书写正确的是
A.在FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
B.向CaCl2溶液中通入二氧化碳气体:Ca2++CO2+H2O=CaCO3+2H+
C.向氨水中加入稀硫酸:H++OH-=H2O
D.醋酸与锌粒反应:2H++Zn2+=H2↑+Zn
第Ⅱ卷(非选择题,共52分)
15、 “神舟六号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池。该电池可同时供应电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2 +O2 =2H2O,负极反应为H2 +CO32- -→ CO2 ↑+H2O+2e-,则下列推断正确的是
A.电池工作时,CO32-向负极移动
B.电池放电时,外电路电子由通氧气的正极流向通氢气的负极
C.正极的电极反应为:4 OH-→O2 ↑+2H2O+2e-
D.通氧气的电极为阳极,发生氧化反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com