
2£Æ∫‚¡øø’∆¯÷ ¡ø∫√ªµµƒ÷∏±Í «(°°°° )
A£ÆNO x°°°° °°°°°°°°°°°°°° B£ÆCO x°°°° °°°°°°°°°°°°°°°° C£ÆAPI°°°°°°°°°°°°°°°°°°°°°°°° D£ÆSO x
1£Æƒ≥»’ƒ≥ – –«¯∏˜œÓŒ€»æŒÔŒ€»æ÷∏ ˝∑÷±Œ™£∫SO2-49£¨NO2-21£¨PM10-23£¨‘Úµ±»’µƒ ◊“™Œ€»æŒÔŒ™(°°°° )
A£ÆSO2°°°° °°°°°°°°°°°°°°°° B£ÆNO2 °°°°°°°°°°°°°°°°°° C£ÆPM10°°°° °°°°°°°°°°°°°° D£Æ∂º≤ª’˝»∑
25£Æ(15∑÷)‘⁄ƒ≥Œ¬∂»œ¬£¨Ω´H2∫ÕI2∏˜0£Æ10molµƒ∆¯Ã¨ªÏ∫œŒÔ≥‰»Î10Lµƒ√б’»ð∆˜÷–£¨∑¢…˙H2 (g)+I2 (g)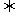 2HI(g)µƒ∑¥”¶£¨¥ÔµΩ∆Ω∫‚∫Û£¨≤‚µ√c(H2)=0£Æ0080mol°§L-1°£
2HI(g)µƒ∑¥”¶£¨¥ÔµΩ∆Ω∫‚∫Û£¨≤‚µ√c(H2)=0£Æ0080mol°§L-1°£
(1)«Û∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝£ª
(2)‘⁄…œ ˆŒ¬∂»œ¬£¨∏√»ð∆˜÷–»ÙÕ®»ÎH2∫ÕI2’Ù∆¯∏˜0£Æ20 mol£¨ ‘«Û¥ÔµΩªØ—ß∆Ω∫‚◊¥Ã¨ ±∏˜ŒÔ÷ µƒ≈®∂»º∞H2µƒ◊™ªØ¬ °£
24£Æ(6∑÷)‘⁄“ª∂®Œ¬∂»œ¬£¨∞—2molSO2∫Õ1molO2Õ®»Î“ª∏ˆ“ª∂®»ðª˝µƒ√б’»ð∆˜¿Ô∑¢…˙»Áœ¬∑¥”¶£∫2SO2(g)+O2(g) 2SO3(g)£¨µ±¥À∑¥”¶Ω¯––µΩ“ª∂®≥Ã∂» ±∑¥”¶ªÏ∫œŒÔæÕ¥¶”⁄ªØ—ß∆Ω∫‚◊¥Ã¨°£œ÷‘⁄∏√»ð∆˜Œ¨≥÷Œ¬∂»≤ª±‰£¨¡Óa°¢b°¢c∑÷±¥˙±Ì≥ı ºº”»ÎµƒSO2°¢O2∫ÕSO3µƒŒÔ÷ µƒ¡ø(mol)£¨»Áπ˚a°¢b°¢C»°≤ªÕ¨µƒ ˝÷µ£¨À¸√«±ÿ–ά˙◊„“ª∂®µƒœýª•πÿœµ≤≈ƒÐ±£÷§¥ÔµΩ∆Ω∫‚ ±£¨∑¥”¶ªÏ∫œŒÔ÷–»˝÷÷∆¯Ãµƒ÷ ¡ø∑÷ ˝»‘∏˙…œ ˆ∆Ω∫‚ ±µƒÕÍ»´œýÕ¨°£«ÎÃÓ–¥œ¬¡–ø’∞◊£∫
2SO3(g)£¨µ±¥À∑¥”¶Ω¯––µΩ“ª∂®≥Ã∂» ±∑¥”¶ªÏ∫œŒÔæÕ¥¶”⁄ªØ—ß∆Ω∫‚◊¥Ã¨°£œ÷‘⁄∏√»ð∆˜Œ¨≥÷Œ¬∂»≤ª±‰£¨¡Óa°¢b°¢c∑÷±¥˙±Ì≥ı ºº”»ÎµƒSO2°¢O2∫ÕSO3µƒŒÔ÷ µƒ¡ø(mol)£¨»Áπ˚a°¢b°¢C»°≤ªÕ¨µƒ ˝÷µ£¨À¸√«±ÿ–ά˙◊„“ª∂®µƒœýª•πÿœµ≤≈ƒÐ±£÷§¥ÔµΩ∆Ω∫‚ ±£¨∑¥”¶ªÏ∫œŒÔ÷–»˝÷÷∆¯Ãµƒ÷ ¡ø∑÷ ˝»‘∏˙…œ ˆ∆Ω∫‚ ±µƒÕÍ»´œýÕ¨°£«ÎÃÓ–¥œ¬¡–ø’∞◊£∫
(1)»Ùa=0£¨b=0£¨‘Úc=_________________°£
(2)»Ùa=0£Æ5£¨‘Úb=________________∫Õc=________________°£
23£Æ(15∑÷)“‘H2°¢O2Œ™‘≠¡œ£¨”√ ؃´◊˜µÁº´£¨KOH◊˜µÁΩ‚÷ »Ð“∫◊È≥…»º¡œµÁ≥ÿ£¨‘Ú¥À»º¡œµÁ≥ÿµƒ∏∫º´∑¢…˙_________________∑¥”¶£ªµÁº´∑¥”¶ ΩŒ™_________________£ª’˝º´∑¢…˙_________________∑¥”¶£ªµÁº´∑¥”¶ ΩŒ™_________________£¨“ª∂Œ ±º‰∫Û£¨»Ð“∫µƒºÓ–‘_________________(ÃÓ°∞‘ˆ¥Û°±°∞ºı–°°±°∞≤ª±‰°±)
22£Æ(2∑÷)“—÷™298K ±£¨C(s)+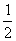 O2==CO(g)°°°° °˜H1=-110£Æ5KJ/mol
O2==CO(g)°°°° °˜H1=-110£Æ5KJ/mol
C(s)+O2(g)=CO2(g)°° °˜H=-393£Æ5 KJ/mol
‘Ú¥ÀŒ¬∂»œ¬£∫CO(g)+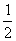 O2(g)=CO2(g)µƒ°˜HŒ™_________________£Æ
O2(g)=CO2(g)µƒ°˜HŒ™_________________£Æ
21£Æ(2∑÷)–¥≥ˆ298K ±£¨3molNO2(g)”Î1molH2O(l)∑¥”¶…˙≥…HNO3(aq)∫ÕNO(g)£¨∑≈»»138kJµƒ»»ªØ—ß∑Ω≥à Ω_________________°£
20£Æ”√∂Ë–‘µÁº´µÁΩ‚M(NO3)xµƒÀƻГ∫£¨µ±“ıº´…œ‘ˆ÷ÿa g ±£¨‘⁄—Ùº´…œÕ¨ ±≤˙…˙b L(±Í◊º◊¥øˆ)—ı∆¯£¨¥”∂¯ø…÷™Mµƒœý∂‘‘≠◊”÷ ¡ø «(°°°° )
A£Æ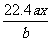 °° °°°°°°°°°°°° B£Æ
°° °°°°°°°°°°°° B£Æ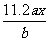 °° °°°°°°°°°°°°°° C£Æ
°° °°°°°°°°°°°°°° C£Æ °° °°°°°°°°°°°°°° D£Æ
°° °°°°°°°°°°°°°° D£Æ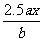
µ⁄¢ÚæÌ(∑«—°‘ÒÂπ≤40∑÷)
19£Æ∂‘”⁄2NO2 N2O4(∑≈»»)£¨‘ˆ¥Û—π«ø(Àı–°Ãª˝)£¨œ¬¡–Àµ∑®’˝»∑µƒ «(°°°° )
N2O4(∑≈»»)£¨‘ˆ¥Û—π«ø(Àı–°Ãª˝)£¨œ¬¡–Àµ∑®’˝»∑µƒ «(°°°° )
A£Æ∆Ω∫‚ƒÊœÚ“∆∂Ø£¨°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£ÆªÏ∫œ∆¯Ã—’…´œ»±‰…Ó∫Û±‰«≥
C£ÆªÏ∫œ∆¯Ã—’…´œ»±‰«≥∫Û±‰…Ó°°°° °°°°°°°°°°°°°° D£ÆªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø±‰–°
18£Æ∂‘”⁄√б’»ð∆˜÷–Ω¯––µƒ∑¥”¶£∫CaCO3(s) CaO(s)+CO2(g)£ª°˜H>0£¨¥Ô∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∂‘∑¥”¶ÀŸ¬ µƒ– ˆ’˝»∑µƒ «( °°°°)
CaO(s)+CO2(g)£ª°˜H>0£¨¥Ô∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∂‘∑¥”¶ÀŸ¬ µƒ– ˆ’˝»∑µƒ «( °°°°)
A£Æ’˝∑¥”¶ÀŸ¬ ‘ˆ¥Û£¨ƒÊ∑¥”¶ÀŸ¬ ºı–°£¨∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø
B£Æ’˝∑¥”¶ÀŸ¬ ºı–°£¨ƒÊ∑¥”¶ÀŸ¬ ‘ˆ¥Û£¨∆Ω∫‚œÚƒÊ∑¥”¶∑ΩœÚ“∆∂Ø
C£Æ’˝ƒÊ∑¥”¶ÀŸ¬ ∂º‘ˆ¥Û£¨∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø
D£Æ’˝ƒÊ∑¥”¶ÀŸ¬ ∂ººı–°£¨∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com