

13.研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物: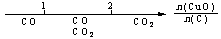
B.Fe在Cl2中的燃烧产物:
C.AlCl3溶液中滴加NaOH后铝的存在形式: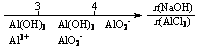
D.氨水与SO2反应后溶液中的铵盐: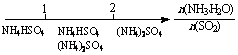
第Ⅱ卷
必考题
12.信息:在治疗甲型流感的疫苗尚未研制面世之前,科学家一直表示,达菲类流感特效药可治疗这种新型流感病毒,它可由我国特有中药材八角的提取物--莽草酸(shikimicacid)为原料合成的。已知莽草酸和达菲的结构式如下:
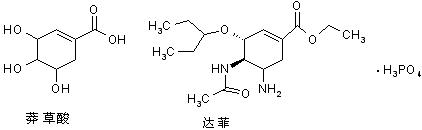
根据题意,下列判断正确的是
A.它们互为同系物
B.莽草酸能使溴的四氯化碳溶液褪色,达菲不能
C.达菲的分子式C16H28N2O4•H3PO4
D.莽草酸与FeCl3溶液显紫色
11.将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是
A.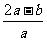 B.
B.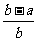 C.
C.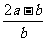 D.
D.
10.一定质量的钠、钾分别投入一定量的稀盐酸中,产生气体随时间变化的曲线如下图所示, 则下列说法中正确的是
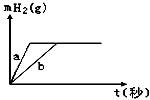
A.投入的Na、K一定等质量 B.稀盐酸的量一定是不足量的
C.曲线a为Na,b为K D.投入的Na的质量小于K的质量
9.下列关于晶体的说法一定正确的是
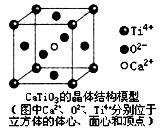
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
8.对下列各种溶液中所含离子的判断合理的是
A.向无色溶液中加氯水变橙色,溶液中可能含:SO42-,Br-,OH-,Ba2+
B.在c(H+)=10-14mol/L的溶液中可能含:Na+,AlO2-,CO32-,SO32-
C.在常温下加入铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3-
D.使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Fe2+,HCO3-
7.下列实验的结果不能用于说明实验目的的是
|
代号 |
实验内容 |
实验目的 |
|
A |
Cl2、Br2分别与H2反应 |
比较氯与溴的非金属性强弱 |
|
B |
向饱和Na2SiO3溶液中通入二氧化碳 |
比较碳与硅的非金属性强弱 |
|
C |
MgCl2、AlCl3溶液中分别通入NH3 |
比较镁、铝的金属性强弱 |
|
D |
向氯化铜溶液中加入铁丝 |
比较铁与铜的还原性强弱 |
24.(10分)通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于_______________________________。
(2)最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
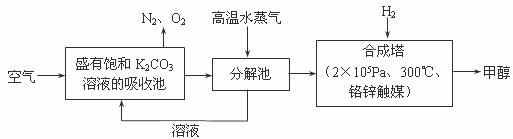
①吸收池中反应的化学方程式为_____________________________________。
②在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,可放出4947 kJ的热量,试写出合成塔中发生反应的热化学方程式________________________________。
(3)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp)分别为4.96×10-9、2.58×10-9。
小李应该选用的试剂是___________________,实验时测定的数据除空气的体积外,还需要测定____________________________________________________________。
23.(15分)化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中Na2CO3的质量分数。
[方案一]
称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为: ;
(2)实验中,需加热至恒重的目的是 。
[方案二]
称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-==BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为 。
(2)实验中判断沉淀是否完全的方法是 。
[方案三]
按如下图所示装置进行实验:
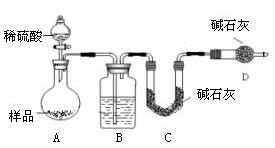
(1)检查装置A的气密性的方法是____________________________________________
(2)D装置的作用是 。
分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(3)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中Na2CO3的质量分数为 。
(4)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是:
_________________________________________________。
22.(12分).在容积为2L的密闭容器中,进行如下反应:
A(g)+2B(g)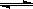 C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
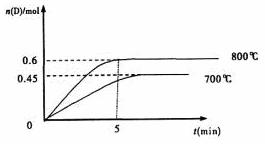
(1)800℃时。0-5min内,以B表示的平均反应速率为 。
(2)能判断该反应达到化学平衡状态的依据是 。
A.容器压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
E.混合气体密度不变
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= ,B的平衡转化率为: 。该反应为 反应(填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=2.2mol,n(B)=5.2mol,n(C)=1.8mol,n(D)=1.8mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com