
2.下列说法中正确的是: ( )
A.分解反应一定是氧化还原反应
B.非金属单质在氧化还原反应中一定做氧化剂
C.氧化剂具有氧化性,还原剂具有还原性
D.氧化剂在化学反应中被氧化
1.下列变化,需加入氧化剂才能实现的是: ( )
A.CO→CO2 B.MnO
B.MnO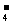 →Mn2+ C.SO2→H2SO3
D.NaCl→AgCl
→Mn2+ C.SO2→H2SO3
D.NaCl→AgCl
21.(6分)生态溶液涉及农家肥的综合利用,某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有炽热的黑色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO→CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。(写解题过程)
(1)原混合气体中甲烷的物质的量是 。
(2)原混合气体中氮气的体积分数为 。
20.(8分)将1mol CO和1mol H2O(g)充入某固定容积的反应器中,在某条件下达到平衡:CO+H2O(g) CO2+H2,此时有
CO2+H2,此时有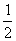 的CO转化为CO2。
的CO转化为CO2。
(1)该平衡混合物中CO2的物质的量分数为 。
(2)温度不变的条件下向该平衡体系中再充入一定量的氩气,CO的转化率
(填“增大”、“减小”、“不变”)
(3)温度不变的条件下向该平衡体系中再充入1mol CO2和1mol H2,则达新平衡时CO2的物质的量分数为 。
(4)若在相同条件下,开始时向容器中充入1mol CO2、1mol H2和1mol H2O,则达到平衡时,混合物中CO2的物质的量分数可能是下列各值中的 (填编号)
A.16.67% B.27.55% C.33.3% D.36.8%
19.(10分)已知短周期元素的单质X、Y、Z在通常状况下均为气态,并存在下列转化关系(反应条件略去):
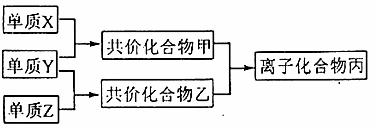
已知:在常见双原子单质分子中,X分子含共价键最多;甲分子含10个电子,乙分子含18个电子。
回答下列问题:
(1)X的结构式是 。
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
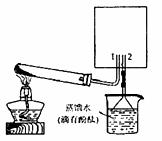
①从下列装置中选出上图方框内收集甲的装置是 。
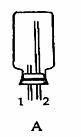
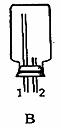
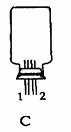
②试管中的试剂是(填写化学式) 。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示) 。
(3)磷在单质Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外电子层均满足8电子结构,丁的化学式是 。
18.(13分)已知B是常见的金属单质,E为常见的气态非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答:
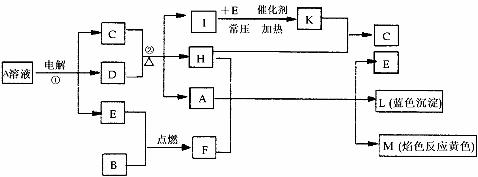
(1)L的化学式为: ;F的电子式为: ,
所含化学键为 ;
(2)反应①的离子方程式为: ;该反应前后溶液的pH (填:“变大”;“变小”;“不变”)
(3)每生成1 mol K,反应放出98.3 kJ的热量,该反应的热化学方程式为: 。
(4)反应②的化学方程式为: ;
(5)化合物F与Na2S溶液反应,生成NaOH和S单质,试写出该反应的离子方程式为 。
17.(15分)D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为 ;
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是 ,写出该元素的任意3种含氧酸的化学式 ;
(3)D和Y形成的化合物,其分子的空间构型为 ;
(4)D和X形成的化合物,其化学键类型属 ,其晶体类型属 ;
(5)金属镁和E的单质在高温下反应得到的产物是 ,此产物与水反应生成两种碱,该反应的化学方程式是 。
(6)试比较D和X的最高价氧化物熔点的高低并说明理由:
16.下图中,两电极上发生的电极反应为:a极:Cu2++2e-= Cu b极:Fe - 2 e-= Fe2+
下列说法中不正确的是( )
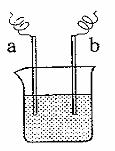
A.该装置可能是电解池
B.a极上一定发生还原反应
C.a、b可能是同种电极材料
D.该过程中能量的转换一定是化学能转化为电能
第Ⅱ卷(非选择题,共52分)
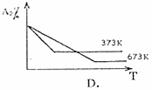
15. 对于可逆反应A2(g)+3B2(g) 2AB3(g);△H<0,下列图像正确的是( )
对于可逆反应A2(g)+3B2(g) 2AB3(g);△H<0,下列图像正确的是( )
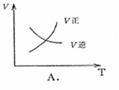
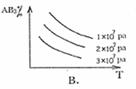
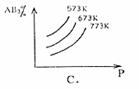
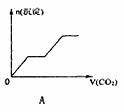
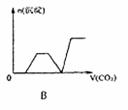
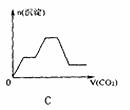
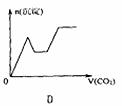
14.将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2体积的关系可表示为 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com