
11.下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,下列说法正确的是 ( )
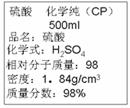
A.该硫酸的物质的量浓度为9.2 mol•L-1
B.配制200 mL 4.6 mol•L-1的稀硫酸需取该硫酸25 mL
C.该硫酸与等体积的水混合后所得溶液浓度为9.2 mol•L-1
D.该硫酸与等体积水混合后质量分数大于49%
10.第三周期元素R,它的原子最外电子层上达到饱和所需电子数小于次外层和最内层电子数之差,但等于最内层电子数的正整数倍。下列说法正确的是 ( )
A.常温下,能稳定存在的R的氧化物都能与烧碱溶液反应
B.R的最高价氧化物对应的水化物都是强酸
C.在固态时,R的单质属于同一类型的晶体
D.在常温下,R的气态氢化物都能在空气中稳定存在
9.一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6 mol/L KOH溶液,下列说法中正确 ( )
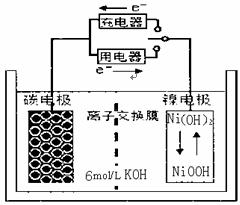
A.放电时K+移向负极
B.放电时电池负极的电极反应为:H2-2e- = 2H+
C.放电时电池正极的电极反应为: NiO(OH)+H2O+e- = Ni(OH)2+OH-
D.该电池充电时将碳电极与电源的正极相连
8.下列离子方程式书写正确的是 ( )
A.向50 mL 1 mol·L-1明矾溶液中滴入数滴0.1 mol·L-1Ba(OH)2溶液
Al3++2SO42-+2Ba2++3OH- === Al(OH)3↓+2BaSO4↓
B.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I- === 3I2+2H2O
C.a mol FeBr2溶液中通入a mol Cl2:2Fe2++2Br-+2Cl2 = Br2+2Fe3++4C1-
D.在澄清石灰水中加入适量碳酸氢镁溶液:Ca2++ OH-+ HCO3- == CaCO3↓+H2O
7.在指定环境中,下列各组离子可以大量共存的是 ( )
A.无色溶液中:[Ag(NH3)2]+、K+、 H+ 、NO3-
B.滴加酚酞试液仍无色的溶液中:CO32-、K+、ClO-、AlO2-
C.在c(H+)/c(OH-) = 1×1013的溶液中:NH4+、Ca2+、C1-、K+
D.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42-
6.碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-。已知在不同温度下该反应的平衡常数如下图,下列说法不正确的是 ( )
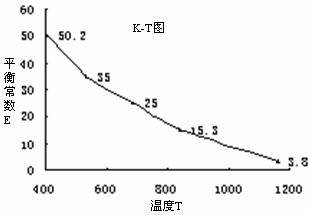
A.上述反应正反应为放热反应
B.实验室配制碘水,为增大碘的溶解度可加入少量的KI
C.用该反应原理可除去硫粉中少量的碘单质
D.上述体系中加入苯,平衡不移动
5.取少量MgO、A12O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,充分反应后过滤,得到沉淀X和滤液Y。下列叙述正确的是 ( )
A.上述四种氧化物对应的水化物中,Al(OH)3酸性最强
B.向沉淀X中逐滴加入硝酸,沉淀慢慢溶解
C.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
D.溶液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2
4.下列装置所示的实验不能达到目的的是 ( )
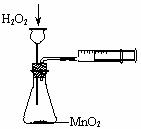
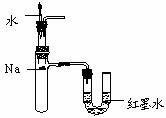
A.定量测定化学反应速率 B.验证Na和水反应的热效应
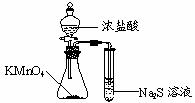
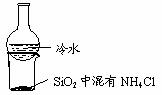
C.比较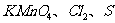 的氧化性 D.加热烧杯,分离
的氧化性 D.加热烧杯,分离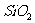 和
和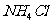
3.下列实验方案能达到目的的是 ( )
A.除去Fe粉中混有的I2:加热使I2升华
B.除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶
C.除去碳酸钠中混有的碳酸氢钠:加入过量的氢氧化钠溶液,蒸发结晶
D.除去氢氧化镁中混有的氢氧化钙:放入水中搅拌成浆状后,加入足量氯化镁溶液,加适量水过滤洗涤
2.设NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.12 g NaHSO4在熔融时离子总数为0.3NA
B.28 g N60单质(见下图)中含有的N-N键个数为3NA

C.在25℃时,压强为1.01×105 Pa时,11.2 L氧气所含的原子数为NA
D.常温下,将5.6 g 铁投入足量的浓硫酸中转移电子数为0.3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com