

26.(4分)相同温度下,1mol·L-1的下列溶液,pH由小到大的是(填序号)
①氨水 ②Na2CO3 ③NaHCO3 ④NaClO ⑤NH4Cl ⑥NaHSO4
25.下图中X、Y分别是直流电源的两极,通电后,发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是 ( )
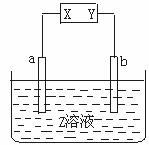
a极板 b极板 X电极 Z溶液
A.锌 石墨 负极 CuSO4
B.石墨 石墨 负极 NaOH
C.银 铁 正极 AgNO3
D.铜 石墨 负极 CuCl2
24.x、y均为短周期元素,且x为ⅠA族元素,y为ⅥA族元素。下列说法正确的是( )
A.x的原子半径一定大于y的原子半径
B.由x、y形成的共价化合物中所有原子都满足最外层为8电子结构
C.x2y既可能是离子化合物,也可能是共价化合物
D.由x、y组成的化合物中,x、y的原子个数比不可能是1:1
23.已知①2H2O(g)== 2H2O(l) H=2Q1 kJ/mol
②C2H5OH(g) == C2H5OH(l) H=3Q2 kJ/mol
③C2H5OH(g) + 3O2(g) == 2CO2(g) + 3H2O(g) H=Q3 kJ/mol
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为(kJ) ( )
A.Q1 + Q2 + Q3 B.0.5(Q1 + Q2 + Q3)
C.0.5Q1 - 1.5Q2 + 0.5Q3 D.1.5Q1 - 1.5Q2 + 0.5Q3
22.下列说法或表示方法正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由H(aq)+OH(aq) = H2O(l); H=57.3kJ/mol可知,若将含1mol CH3COOH稀溶液与含1mol NaOH的稀溶液混合,放出的热量小于57.3kJ
C.由C(石墨,s)== C(金刚石,s) H= + 1.90kJ/mol可知,金刚石比石墨稳定
D.在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g) + O2(g) == 2H2O(l) H=285.8 kJ/mol
21.实验室用铅蓄电池电解饱和食盐水制取氯气,今若制得Cl2 0.05mol,这时电池内消耗的H2SO4的物质的量至少是 ( )
A.0.025mol B.0.050mol C.0.10mol D.0.20mol
20.常温下,把pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系正确的是 ( )
A.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.c(Na+)+c(H+)>c(CH3COO-)+c(OH-)
C.c(CH3COO-)>c(Na+)>c(H+)=c(OH-)
D.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
19.把3mol A和1mol B混合于体积不变的密闭容器中发生反应:3A(g) + B(g) ==2C(g)+ D(g),达到平衡时,C的体积百分含量为w%。若在相同条件下,把2molC和2molD混合于相同体积的密闭容器中反应,达到平衡后,混合气体中C的体积百分含量为 ( )
A.大于w% B.小于w% C.等于w% D.无法判断
18.对于aA(g)+bB(g)==cC(g)+dD(g)的平衡体系,如下图,纵坐标代表D的百分含量,下列判断正确的是 ( )
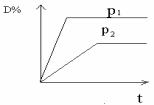
A.P1 < P2 a+b < c+d B.P1 < P2 a+b > c+d
C.P1 > P2 a+b < c+d D.P1 > P2 a+b > c+d
17.250C时,pH = 3的盐酸溶液中由水电离出的c(H+)是pH = 5的NH4Cl溶液中由水电离出的c(H+)的( )倍
A.10-2 B.10-6 C.2 D.106
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com