
29.(12分)钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3·xH2O),反应的化学方程式:
。
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式 。
(3)下列哪个装置可防止铁棒被腐蚀_____________ 。
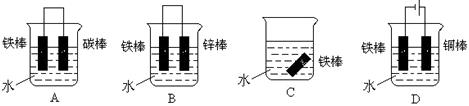
(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:
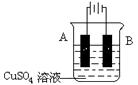
请回答:
①B电极的电极反应式是 。
②若电镀前铁、铜两电极质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为1.92 g,则电镀时电路中通过的电子为________________mol。
(5)钢铁“发蓝”是在钢铁表面形成一层致密的Fe3O4薄膜的技术。其中一种方法是将钢铁制品浸到NaNO2和浓NaOH的混合溶液中加热到130℃。其过程可以用如下化学方程式表示:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH
整个反应过程中,每转移4mol电子,有 g Fe参加反应。
28.(14分)A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件及部分产物未列出)。

(1)若A是常见金属单质,与B的水溶液反应生成C和D。D、F是气体单质,D在F中燃烧时发出苍白色火焰。则反应②(在水溶液中进行)的离子方程式为 。
(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属。且③④两个反应都有红棕色气体生成,则反应④的化学方程式为: 。
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,E溶液中滴加KSCN溶液呈血红色。则D的电子式是 ;工业上生产B的第一个生产阶段是煅烧与A含相同元素的矿石,其煅烧矿石的化学方程式是 ,使用的设备是 。
(4)若B是由地壳中含量最高的两种元素组成,A的一种同素异形体与B、D属同一种类型的晶体,则反应①的化学方程式是 ,B与烧碱溶液反应的离子方程式是 。
27.(16分)2004年,国家食品监督局发出“警惕食品中丙烯酰胺(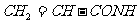 )的公告,丙烯酰胺具有中等毒性,它对人体可造成神经毒性和遗传毒性。已知有机物H是丙烯酰胺的相邻同系物,A为气态烃,标准状况下密度为2.5g
/ L;F为六元环状化合物。回答下列问题:
)的公告,丙烯酰胺具有中等毒性,它对人体可造成神经毒性和遗传毒性。已知有机物H是丙烯酰胺的相邻同系物,A为气态烃,标准状况下密度为2.5g
/ L;F为六元环状化合物。回答下列问题:
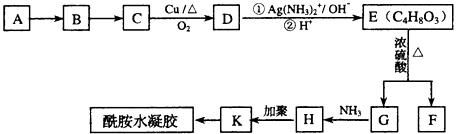
(1)写出G的结构简式____________________、K的结构简式_____________________
(2)指明下列反应类型:A→B、___________________E→G;___________________;
(3)写出下列化学方程式:
C→D________________________________________________________________
E→F________________________________________________________________
(4)下列关于丙烯酰胺的说法,不正确的是________;
①丙烯酰胺可以溶于有机溶剂
②人们应改善膳食习惯,少食油炸食品
③丙烯酰胺有毒,人们要杜绝使用
(5)写出有机物H的同种类别的同分异构体的结构简式:_____________、______________
26.(18分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。
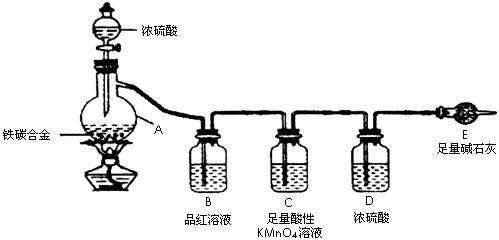
I、测定铁的质量分数:
(1)称量E质量,并按图示连接装置;
(2)需不需要检查装置的气密性?_______(填“需要”或“不需要”);装置C的作用是_____________________________________________________________;
(3)将a g铁碳合金样品放入A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g,铁碳合金中铁的质量分数为_________________(写表达式)
(4)某同学认为:依据此实验装置,计算合金中铁的质量分数可能会偏低,你认为可能的原因是____________________________________________________________。经过大家的讨论,决定采用下列装置和其他常用实验仪器测定某些数据即可,为了快速和准确的计算出铁的质量分数,最简便的实验操作__________________________(填写代号)。

①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③测定反应前后装置和药品的总质量
Ⅱ、探究浓硫酸的某些性质:
(5)未点燃酒精灯前,A、B均无明显现象,其原因是____
点燃酒精灯一段时间后,A、B中可观察到明显的现象,B中的现象是___
写出A中刚开始发生反应的化学方程式:______ 、
_ __。
13.向某二价金属M的M(OH)2的溶液中加入过量的NaHCO3溶液,生成了MCO3沉淀,过滤,将沉淀置于足量的稀盐酸中,充分反应后,在标准状况下收集到V L气体。如要计算金属M的相对原子质量,你认为还必需提供下列哪项数据( )
A.M(OH)2溶液的物质的量浓度和体积
B.与MCO3反应的盐酸的物质的量浓度和体积
C.MCO3的质量
D.题给条件充足,不需要再补充数据
第Ⅱ卷
12.恒温恒容条件下,下列叙述正确的是( )
A.甲、乙两容器中分别加入1gSO2、1gO2与2gSO2、2gO2,反应2SO2(g)+O2(g) 2SO3(g)达到平衡,SO2的转化率前者大
2SO3(g)达到平衡,SO2的转化率前者大
B.反应2HI(g) H2(g)+I2(g)达平衡,增大HI的物质的量,平衡不移动
H2(g)+I2(g)达平衡,增大HI的物质的量,平衡不移动
C.反应2HI(g) H2(g)+I2(g)达平衡,增大HI的物质的量,HI分解率不变,体积分数不变
H2(g)+I2(g)达平衡,增大HI的物质的量,HI分解率不变,体积分数不变
D.反应2NO2(g) N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数增大
N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数增大
11.下列各项判断正确的是( )
A.溶液中溶质浓度均为0.1mol/L的下列溶液:①H2S ②NaHS ③Na2S ④NaHS和H2S, 其溶液的PH从大到小为:③>②>①>④
B.溶液中溶质浓度均为0.1mol/L的:①H2S ②NaHS ③Na2S ④NaHS和H2S,其溶液中C(H2S)从大到小为:①>④>②>③
C.0.1mol/L PH为4的NaHB的溶液中,C(HB-)>C(H2B)>C(B2-)
D.C(NH4+)相等的下列溶液:①(NH4)2SO4 ②NH4)2CO3 ③NH4Cl其溶质的物质的量浓度的大小关系为:① < ② < ③
10.下列离子方程式正确的是( )
A.在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解:
BaSO3+2H++2NO3-==BaSO4↓+2NO↑+H2O
B.碳酸氢铵与其等物质的量的NaOH 溶液混合:
NH4++HCO3-+2OH-==CO32-+NH3·H2O+2H2O
C.甲酸溶液与NaOH溶液反应:COOH-+OH-==H2O +COO-
D.用小苏打治疗胃酸过多:HCO3-+H+==CO2↑+H2O
9.波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音。波立维属于硫酸氢盐,它的结构如图所示。下列关于它的说法正确的是( )
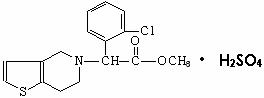
A.该物质的化学式为C16H15SClNO2·H2SO4
B.该物质不溶于水
C.它可以与NaOH溶液反应,1mol该物质最多可消耗4molNaOH
D.波立维能和氢气反应,每摩最多可消耗3摩氢气
8.下列文字表述与反应方程式对应且正确的是( )
A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+ AgBr↓
AgBr↓
B.用醋酸除去水垢:CaCO3
+ 2H+ Ca2+
+ H2O + CO2↑
Ca2+
+ H2O + CO2↑
C.溴水和苯制溴苯: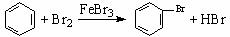
D.碳酸氢钠和偏铝酸钠溶液离子反应:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com