
1.下列叙述正确的是
A.△H>0且△S<0的反应一定能自发进行
B.常温下,PH=1的水溶液中,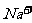 、
、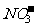 、
、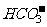 、
、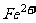 可以大量共存
可以大量共存
C.明矾和漂白粉用于自来水的净化和杀菌消毒,两者的作用原理相同
D.C(石墨,s)=C(金刚石,s);△H>0,所以石墨比金刚石稳定
(二)选考题。
35.[化学--选修--有机](12分)
Ⅰ.相对分子质量不超过100的有机物N,既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 N完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。经核磁共振检测发现N的氢谱如下:

(1)N的结构简式为:___________________________________。
Ⅱ.塑料是常用的合成高分子材料,常用塑料F、G均可由某烃经下列反应得到:
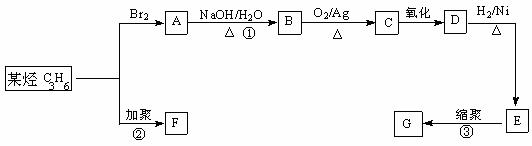
(2)写出反应①的化学方程式:_______ _________________________;
(3)写出反应②的化学方程式:_______ _________________________;
(4)写出反应③的化学方程式:_______ _________________________;
36.[化学--选修--物质结构与性质](12分)
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层中P轨道上的电子数等于前一电子层电子总数,X原子最外层的P轨道中有一个轨道填充了2个电子。则
(1)X原子的电子排布式是 ,Y原子的价层电子轨道表示式是 。
(2)YX2的分子构型是 ,YX2的熔沸点比ZX2 ,(选填“高”或“低”),理由是
(3)YX2分子中,Y原子的杂化类型是 ,一个YX2分子中含 个π键。
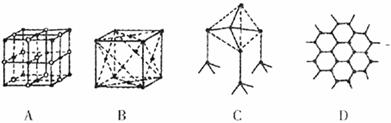
(4)下图表示一些晶体的结构(晶胞),其中代表YX2的是
26.(13分)X、Y、Z为三种不同短周期非金属元素的单质。在一定条件下发生如下反应:
请针对以下两种不同的情况回答:
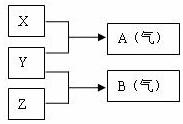
(1)若常温下X、Y、Z均为气体,且A和B在化合生成固体C时有白烟产生,则:
①Y的化学式是 ;
②生成固体C的化学方程式是 。
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式为 ;
②向苛性钠溶液中通入过量的A所发生反应的离子方程式为 ;
③将B与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式为 。
27.(13分)物质之间的转化关系如下图所示,A可作为工业生产J的原料,B、C、H、I为非金属单质,H是密度最小的气体,X的水溶液为一种常见的无色医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见的含碳氮肥,且反应⑦中L与M的物质的量之比为1∶2,A、E、J、N中含有同一种元素.
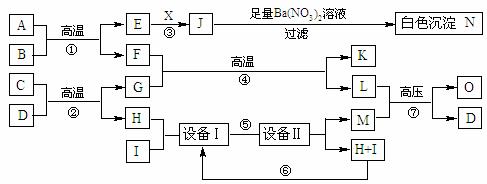
回答下列问题:
(1)X的化学式为_______________,C+D的反应方程式为___________________.
(2)设备Ⅰ的名称_______________.工业生产中为了节约资源、降低成本和保护环境,常常对某些物质进行循环利用.上述转化关系中能达到该目的的步骤是__________(填序号)
(3)现有1molA参加反应,假设各步反应均完全,生成N的质量为1165g,生成K的质量为224g,则反应①的化学方程式为___________________________.
28.(20分)实验室用燃料法测定某种氨基酸(CxHyOzNp)的分子式组成,取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出)。请回答有关问题:
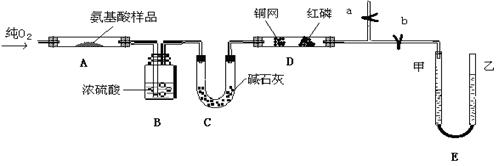
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通入一段时间的氧气,这样做的
目的是 ,之后关闭止水夹a。
(2)由装置B、C可分别确定待测氨基酸中含有的 和 质量。
(3)E装置的作用是测量 的体积,并由此确定待测氨基酸中含有的 。
的质量,为了较准确地测量该气体的体积。在读反应前后甲管中液面的读数求其差值的过程中,应注意 (填代号)。
A.视线与凹液面最低处相平
B.等待片刻,待乙管中液面不再上升时,立刻读数
C.读数时应上下移动乙管,使甲、乙两管液面相平
D.读数时不一定使甲、乙两管液面相平
(4)实验中测定的哪一数据可能不准确
其理由是
(5)严格地说,按上述方案只能确定氨基酸的 。
若要确定此氨基酸的分子式,还要测定该氨基酸的 。
13.现有碳酸钠、碳酸氢钠、氢氧化钠、氯化铁和苯酚五种物质的溶液,它们之间有如图所示转化关系,图中每条线两端的物质均可以发生反应,下列判断不合理的是 ( )
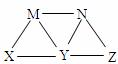
A.X一定是碳酸氢钠溶液
B.Y一定是氯化铁溶液
C.Z可能为碳酸钠溶液
D.M、N必定各为苯酚、氢氧化钠溶液中的某一种
第Ⅱ卷
12.下列关于实验问题处理方法或操作不正确的是 ( )
A.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
B.中和滴定前,锥形瓶内含少量水
C.中和热测定中要用稍过量的酸(或碱),以便使碱(或酸)能够完全被中和
D.配制稀硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
11.100gC不完全燃烧所得产物中,CO所占体积为1/3,CO2为2/3,且:
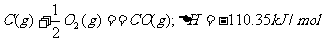
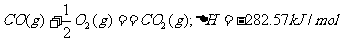
与这些碳完全燃烧相比,损失的热量为 ( )
A.39.292kJ B.3274.3kJ C.784.92kJ D.2489.44kJ
10.在容积不变的密闭容器中存在如下反应:
2SO2(g)+O2(g)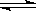 2SO3(g);△H=-196.6kJ·mol-1
2SO3(g);△H=-196.6kJ·mol-1
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是 ( )
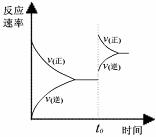
A.图I研究的是t0时刻增大O2的浓度对反应速率的影响
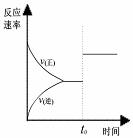
B.图II研究的是t0时刻加入催化剂后对反应速率的影响
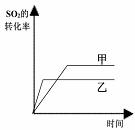
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且乙的温度较低
9.某溶液中有Ca2+、Mg2+、Fe2+和Al3+四种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量的盐酸,溶液中大量减少的阳离子是 ( )
A.Ca2+ B.Mg2+ C.Fe2+ D.Al3+
8.下列反应的离子方程式正确的是 ( )
A.次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+ H2O
+CO2==CaCO3↓+2HClO
B.硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+=Fe3++4H2O
C.用氨水吸收少量二氧化硫 NH3·H2O +SO2=NH4++HSO3-
D.硝酸铁溶液中加过量氨水 Fe3++3NH3·H2O ==Fe(OH)3↓+3 NH4+
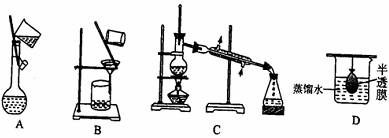
7.以下实验装置一般用于分离互溶的液体物质的是 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com