
3.下列说法正确的是 ( )
A.两难溶电解质作比较时,Ksp小的,溶解度一定小;
B.Ksp大小取决于难溶电解质的量,所以离子浓度改变时,沉淀平衡会发生移动
C.所谓沉淀完全就是用沉淀剂将溶液中某一离子除净;
D.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,此溶液为AgCl的饱和溶液
4.下列涉及有机物的性质或应用的说法不正确的是 ( )
A.干馏煤可以得到甲烷、苯和氨等重要化工原料
B.用于奥运“祥云”火炬的丙烷是一种清洁燃料
C.用大米酿的酒在一定条件下密封保存,时间越长越香醇
D.油脂都不能使溴的四氯化碳溶液褪色
5.元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是 ( )
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最强
D.同周期元素中Y的最高价含氧酸的酸性最强
2.吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”,中国科学家尝试用Na2SeO3清除人体内活性氧,则Na2SeO3的作用是 ( )
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.以上均不是
1.广州将于2010年承办第16界亚运会。下列措施有利于节能减排、改善环境质量的有( )
①在大亚湾核电站已安全运行多年的基础上,广东将继续发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁、轻轨等轨道交通,促进珠三角城市一体化发展,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾
A.①②③④  B.①②⑤
C.①②④⑤ D.③④⑤
B.①②⑤
C.①②④⑤ D.③④⑤
2.每小题选出答案后,用铅笔把答题卡上对应的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其它答案。不能答在答题纸上。
相对原子质量:H:1 C:12 N:14 O:16 Na 23 Mg 24 Al 27 S 32 Ba 127
第Ⅰ卷(选择题,共40分)
选择题(本题包括16小题,1至8题每题2分,9至16题每题3分,共40分,每小题只有一个正确选项。)
1.答题前,考生必须将自己的姓名、考号、考试科目、试卷类型(A)用铅笔涂写在答题卡上。
21.(12分)[本题包括两个选做题,考生从中选择一个作答] [化学--有机化学基础]
有机物A是有机合成的中间体,分子中含2个氧原子,其燃烧产物n(CO2):n(H2O)=2:1;质谱图表明A的相对分子质量为188;在一定条件下A可以转变为B和C(分子式:C4H6O),相关转化关系如下图所示
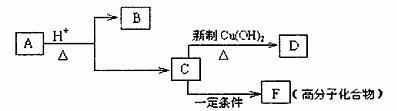
已知:①R-CH=CH-OH会自动转化为R-CH2-CHO;
②同一个碳原子上连有两个双键的结构不稳定;
③B苯环上的一氯取代物有两种同分异构体;C分子中无支链。
请根据以上信息,回答下列问题:
(1)A的分子式是 ,B中含氧官能团的名称是 ,F的结构简式是 。
(2)写出由C生成D的化学方程式: ;
(3)C有多种同分异构体,其中与C具有相同官能团的同分异构体(不含C)共有 种。
(4)上述转化过程中不涉及的有机反应类型有 (填序号)。
①取代反应 ②聚合反应 ③消去反应 ④氧化反应 ⑤还原反应
⑥水解反应
[化学--物质结构与性质] 
A、B、C、D分别代表四种不同的短期周元素。A元素原子的最外层电子排布为ns1,B元素原子的价电子排布为ns2np2,C元素原子的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P轨道中有3个电子。
(1)C原子的价电子排布式为 ,若A元素的原子最外层电子排布为1s1,则按原子轨道的重迭方式,A与C形成的化合物中的共价属于 键。
(2)当n=2时,B与C形成的晶体属于
晶体;当n=3时,B与C形成的晶体中微粒间的作用力是
。
(3)若A元素原子的最外层电子排布为2s1,B元素原子的价电子排布为3s23p2,元素A在周期表中的位置是 ,A、B、C、D四种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
20.(12分)新华社2009年10月15日报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更好更快地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101kPa时:C(s)+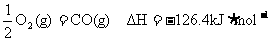
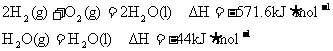
则在25℃,101kPa时:C(s)+H2(g)=CO(g)+H2(g)△H= 。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g)=Fe(s)+CO2(g)△H>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K的值 (填“增大”、“减小”或“不变”)
②1100℃时测得高炉中,c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1,则在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为: CO2(g)+3H2(g)==CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
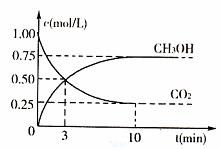
①从反应开始到平衡,氢气的平均反应速率v(H2)= ;
②下列措施能使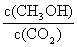 增大的是 (填符号)。
增大的是 (填符号)。
A.升高温度 B.再充入H2
C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
19.(12分)某化学过程的示意图如图所示。在装置工作过程中,甲池的总反应式为:
2CH3OH+3O2+4NaOH=2Na2CO3+6H2O。试回答下列问题:
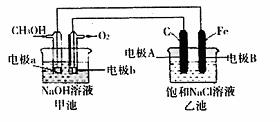
(1)甲池溶液中的Na+移向 (填“a”或“b”)电极,乙池溶液中的Na+移向 (填“A”或“B”)电极;
(2)电极A的名称: ;
(3)电极b上发生的电极反应式为 ;
(4)乙池中发生反应的离子方程式为 ;
(5)当电极A处得到0.71g产物时,甲池中理论上消耗O2 mL(标准状况下)。
18.(12分)W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的某种原子没有中子;Y与X相邻,Y与Z也相邻,X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高。 试回答下列问题:
(1)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,写出其中两种离子发生反应生成其中两种分子的离子方程式 。
(2)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A和B是日常生活中常用调味品的主要成分,且A与B能够反应生成C,试写出该反应化学方程式 。
(3)由W、X、Y、Z四种元素的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式 。
(4)由元素X和Z可组成A、B、C、D四种中学化学常见的单质或化合物,四种物质之间存在如下图所示的转化关系。
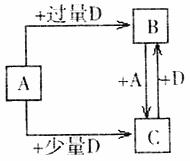
①写出A与B反应生成C的化学方程式 。
②向50mL 4mol·L-1的NaOH溶液中通入1.12L气体B(标准状况),反应后溶液中溶质的物质的量之比为 。
(5)W、Y、Z三种元素可组成一种无机盐,其组成可表示为W4Y2Z3。该盐溶液中离子浓度由大到小的顺序为 。
17.(12分)化学是一门以实验为基础的自然科学,掌握实验方法以及完成化学实验所必须的技能是学好化学的关键。试回答下列实验问题:
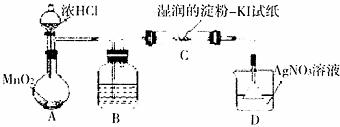
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证。最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀(部分夹持装置和加热装置省略)
①装置B中的试剂是 ;
②装置C的作用是 。
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分为Ag/α-Al2O3)来回收金属银和α-Al2O3,部分操作过程省略。α-Al2O3作为催化剂的载体,且不溶于硝酸。
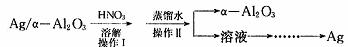
①Ag/α-Al2O3加HNO溶解可选用下图所示装置中的 (选填a、b、c);
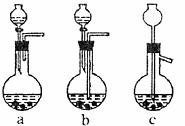
②实验操作II中,所需的主要玻璃仪器有 ;
③实验操作II中能否用自来水代替蒸馏水? (填“能”或“否”);原因是
(结合有关离子方程式回答)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com