
7.地球上,一切生命活动起源于水。下列有关水的物理量中,不随水的体积变化而变化的是
A.水的物质的量 B.水的摩尔质量
C.水的质量 D.所含水分子的数目
6.将5mol/L盐酸10 mL稀释到200 mL,从中取出5mL。这5mL溶液的物质的量浓度为
A.0.5mol/L B.0.25mol/L C.0.1mol/L D.1mol/L
5.下列各组物质中,分子数相同的是
A.2L SO2和2L CO2 B.9g水合标准状况下11.2LCO2
C.标准状况下1mol氧气和22.4L水 D.0.2mol H2S和2.24L HCl
4.化学概念是列化学现象与事实的总结和概括。下列说法中正确的是
A.分散系只包括溶液和胶体
B.丁达尔效应是光线通过胶体时能看到光亮的“通路”的现象
C.单位物质的量的物质所具有的质量叫摩尔质量。摩尔质量与1mol物质的质量完全相同
D.物质失电子的反应为还原反应
3.从平时学生实验中我们发现,同学们在进行实验时,出现许多不正确的操作方式,希望同学们在今后的实验中,应该克服不规范的操作。请找出下列图示中正确的实验操作

A.除去CO的CO2 B.萃取时振荡混合液
C.稀释浓硫酸 D.向试管中滴加液体
2.下列实验操作中错误的是
A.用规格为10mL的量筒量取6mL的液体
B.用药匙或者纸槽把粉末状药品送入试管的底部
C.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D.如果没有试管夹,可以临时手持试管给固体或液体加热
1.下到实验操作均要用玻璃棒,其中玻璃棒作用相同的是
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
B.①和③ C.③和④ D.①和④
20.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选择其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.(12分)A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
|
元素 |
结构或性质信息 |
|
T |
基态原子的L层上s电子数等于p电子数 |
|
X |
基态原子最外层未成对电子数在该元素所在周期中最多 |
|
Y |
基态原子的第一电离能在该元素所在周期中最小 |
|
Z |
单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
请根据信息回答有关问题(答题时如需表示具体元素,请用相应的元素符号):
(1)T、X、Y三种元素的电负性由大到小的顺序是 。
(2)写出与X单质分子互为等电子体的物质的化学式 、 。(分子、离子各一种)
(3)X的氢化物分子间能形成氢键,Z的氢化物分子间不易形成氢键,原因是 。
(4)元素Q的原子序数是Y与Z的原子序数之和。
①元素Q基态原子的价电子层电子排布式为 。
②元素Q与元素T、X能形成平面型的[Q(TX)4]2-离子。其中Q与TX-之间的化学键类型为 ,TX-中T原子采用的轨道杂化方式是 。
③Q单质的晶胞如图所示,Q单质中与Q原子的配位数为 。
B.某研究性学习小组拟从实验室含碘废液中回收碘。制订两种方案提取,他们的实验方案如下:
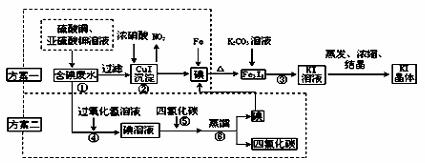
试回答下列问题
(1)方案一,说明废水含有单质碘可用的试剂是:
(2)方案一,步骤③反应的化学方程式为:
(3)方案二,用H2O2而不用Cl2,理由是:
(4)方案二,步骤⑤的名称是:
(5)方案二,蒸馏时用到的玻璃仪器,除接受器、锥形瓶、酒精灯外,还缺少的玻璃仪器有
(6)方案一,②中产生的NO2要进行循环利用,用一总反应式表示这一过程: .
19.(8分)硫酸钙是一种用途非常广泛的产品。
(1)已知25℃时,Ksp(CaSO4)=7.10×10-5。在1L0.1mol·L-1CaCl2溶液中加入1L0.2mol·L-1的Na2SO4溶液,充分反应后(假设混合反溶液的体积变化忽略不计)溶液中Ca2+物质的量浓度为 mol·L-1。
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验;将固体放在坩埚中加热,经测量剩余固体质量随时间变化如图所示。
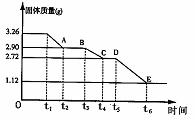
则x:y= 。t2~t3时间段固体的化学式为 。t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色。则该时间所发生反应的化学方程式为 。
18.(13分)
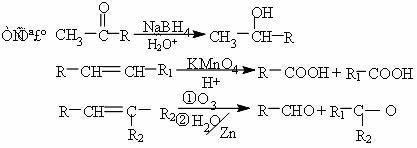
有机物Q只含碳、氢、氧三种元素,分子中碳、氢、氧原子个数比为7:10:3,Q具有酸性;1molQ需要1mol氢氧化钠完全中和;1molQ可以和1molBr2加成,以测定Q的相对分子质量不大于150。各有机物的转化关系如图所示。
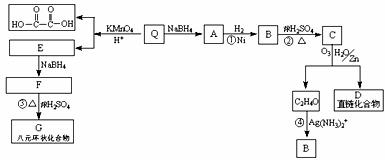
回答下列问题:
(1)写出Q的结构简式 。
(2)反应(8)的反应类型是 。
(3)A-F六种物质中含有手性碳原子的是 (用字母填写)。
(4)写出一种符合下列条件的D的同分异构体的结构简式 。
①能发生银镜反应 ②能发生水解反应 ③结构中无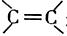 和环状结构
和环状结构
(5)写出一定条件下F生成高分子化合物的反应方程式 。
(6)丙酮酸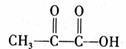 是E的最简单的同系物。
是E的最简单的同系物。
试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件) 。
提示:①合成过程中无机试剂任选;②合成路线流程图示例如下:
CH3CH2OH H2C=CH2
H2C=CH2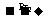 BrH2C-CH2Br
BrH2C-CH2Br
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com