
26. (10分)(1)原子数相同、电子总数相同的分子,互称为等电子体,CO与N2互为等电子体。Fe、Co、Ni等金属能与CO反应的原因与这些金属原子的电子层结构有关。Ni原子的价电子排布式为
。Fe(CO)5常温下呈液态,熔点为-
请完成下列填空:
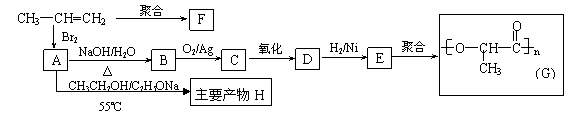
①写出结构简式:聚合物F是 ,产物H ;
②B转化为C的化学方程式为: ;
③在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简是 。
 |
X为Cl 65% 35%
X为Br 75% 25%
X为I 80% 20%
⑴根据上面两个反应的条件及其数据,请写出你认为最具概括性的两条结论:① 。
②
。
⑵由丙烯经下列反应可制得化工原料H及F、G两种高分子化合物(它们都是常用的塑料),其合成线路如下:
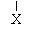 (?)CH3CH2CHCH3――――――→ CH3CH==CHCH3+ CH3CH2CH==CH2+HX
(?)CH3CH2CHCH3――――――→ CH3CH==CHCH3+ CH3CH2CH==CH2+HX
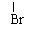 (?)CH3CHCH3 ――――――――→CH3CH==CH2 +
(CH3)2CHOC2H5+HBr
(?)CH3CHCH3 ――――――――→CH3CH==CH2 +
(CH3)2CHOC2H5+HBr
|