
(5)酸性物质使沉淀溶解平衡Ca5(PO4)3OH(s) 5Ca2+(aq)+3PO43 -(aq)+OH-(aq)向右移动,
5Ca2+(aq)+3PO43 -(aq)+OH-(aq)向右移动,
导致Ca5(PO4)3OH溶解,造成龋齿
23、(1)①10NH4NO3; 3H2O。 ②Ca5(PO4)3OH↓+9H2O。
(2)唯一副产物为水,工艺简单。
(3)反应液局部酸性过大,会有CaHPO4产生。 (4)Ca5(PO4)3OH。
(3)3.6 mol< n (SO3)≤4 mol
22、(1)3.6 mol (2)≥0 (说明:答“任意值”可得分)
21、
⑴ 2 5 8 5 2 5 ;
⑵ 2 2 1 4 ;
⑶ 6 3 3 2 4 3 。
25.将N2和 H2按一定比例混合,在相同状况下其密度是H2的 3.6倍,取0.5mol该混合气体通入密闭容器内,使之发生反应并在一定条件下达到平衡。已知反应达到平衡后容器内压强是相同条件下反应前压强的0.76倍,试求:
(1)反应前混合气体中N2和 H2的体积比;
(2)达到平衡时混合气体中的氨的体积分数;
(3)平衡时N2的转化率。
高二年级 化学 答案
题号
1
2
3
4
5
6
7
8
9
10
答案
B
A
C
C
D
D
D
A
B
B
题号
11
12
13
14
15
16
17
18
19
20
答案
D
B
A
C
A
B
A
C
B
B
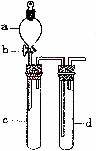
(24图)
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)题表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象为 ;但此实验的不足之处是 。
24.某兴趣小组设计出24图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
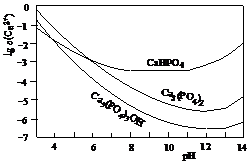
3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3?H2O=Ca5(PO4)3OH↓+__________+_________
②5Ca(OH)2+3H3PO4=_________________________________________
(2)与方法A相比,方法B的优点是__________________________________________。
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是________________________________________。
(4)图中所示3种钙盐在人体中最稳定的存在形式是______________________(填化学式)。
(5)糖黏附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因________________
方案
反应物
甲
Cu、浓HNO3
乙
Cu、稀HNO3
丙
Cu、O2、稀HNO3
23.羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料,其常用的制备方法有两种:
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com