
3ЃЎ25ЁцЃЌдк0.1mol/L NaXШмвКжаЃЌЫЎЕФЕчРыЖШЮЊa1ЃЛдк0.1mol/LбЮЫсжаЃЌЫЎЕФЕчРыЖШЮЊa2ЃЌШєa1/a2=109ЃЌдђNaXШмвКЕФpHдМЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ [ЁЁЁЁЁЁ ]
AЃЎ5ЁЁ BЃЎ7ЁЁ CЃЎ10ЁЁ DЃЎ11
2ЃЎХЈЖШЮЊ0.1mol/LЕФЯТСаИїЮяжЪЕФШмвКжаЃЌ[NH4+]зюДѓЕФЪЧЁЁЁЁЁЁЁЁ [ЁЁЁЁЁЁ ]
AЃЎNH4Cl
BЃЎNH4HSO4
CЃЎNH3?H2O
DЃЎCH3COONH4
DЃЎ0.1mol/LNa2SO4
CЃЎ0.2mol/LKCl
BЃЎ0.1mol/LNa2CO3
AЃЎ0.2mol/LCuSO4
1ЃЎЕШЬхЛ§ЯТСаШмвКжаЃЌбєРызгЕФзмЮяжЪЕФСПзюДѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ [ЁЁЁЁЁЁ ]
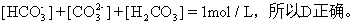
Д№АИЮЊAЁЂDЁЃ
ЁОЭЖгАЁПР§10
вбжЊвЛШмвКжагаЫФжжРызгЃКX+ЁЂY-ЁЂH+ЁЂOH-ЃЌЯТСаЗжЮіНсЙћПЯЖЈДэЮѓЕФЪЧЁЁ [ЁЁЁЁЁЁ ]
AЃЎ[Y-]ЃО[X+]ЃО[H+]ЃО[OH-]
BЃЎ[X+]ЃО[Y-]ЃО[OH-]ЃО[H+]
CЃЎ[H+]ЃО[Y-]ЃО[X+]ЃО[OH-]
DЃЎ[OH-]ЃО[X+]ЃО[H+]ЃО[Y-]
ЬжТлЗжЮіЃК
ЬтФПжаЫФжжРызгдкШмвКжавЛЖЈДцдкЕчКЩЪиКуЁЃ
МД[X+]+[H+]=[Y-]+[OH-]ЃЌ
ИљОнДЫЕШЪНЗжЮіЫФИібЁЯюЃЌ
ЖдAбЁЯю[Y-]ЃО[X+]ЃЌБига[H+]ЃО[OH-]ЃЛ
ЖдBбЁЯю[X+]ЃО[Y-]ЃЌБига[OH-]ЃО[H+]ЃЌВХФмЪЙЕШЪНГЩСЂЃЛ
ЖдCбЁЯю[H+]ЃО[Y-]ЃЌБига[OH-]ЃО[X+]ЃЌЫљвдCбЁЯюДэЮѓЃЛ
ЖдDбЁЯю[OH-]ЃО[X+]ЃЌБига[H+]ЃО[Y-]ЃЌетбљЕШЪНГЩСЂЁЃ
Д№АИЮЊCЁЃ
ЁОЙщФЩЁП
ЕчНтжЪШмвКжаРызгХЈЖШДѓаЁЕФБШНЯОЁЙмИДдгЃЌЕЋНтЬтЙиМќЪЧзЅзЁЦНКтжїЯпЃЌШЯецЗжЮіВЂАДееРызгЕФЕчКЩЪиКуЃЌЮяСЯЪиКуЃЈдЊЫиЕФдзгЪиКуЃЉРэЧхЙиЯЕЃЌОЭПЩПьЫйНтД№ЁЃ
ЁЁ
ОЋбЁЬт
ЁЁ
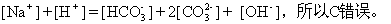
ИљОнЬМдЊЫиЕФдзгЪиКуЃК
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com