
3.在下列4种化合物:①NaHCO3,②Al2O3,③(NH4)2S,④NH2CH2COOH中,跟盐酸和氢氧化钠溶液都能反应的是 ( )
A.只有②、④
B.只有①、②
C.只有①、②、③
D.①、②、③、④
2.某溶液中含有NH4+、Mg2+、Fe2+、Al3+4种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是 ( )
A.NH4+ B. Mg2+
C.Fe2+ D. Al3+
1.某铁的氧化物用1.4 mol?L-1盐酸50mL恰好溶解,所得溶液还能和56mL(标准状况下)Cl2反应,那么该氧化物的化学式为
( )
A.Fe2O3 B.Fe3O4
C.Fe4O5 D.Fe5O7
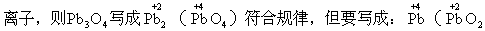

)2则不符合规律。
③Fe3+不能氧化HCl,所以Fe3O4与HCl反应生成两种盐,属于复分解反应;而Pb4+有强氧化性,能把HCl氧化成Cl2,这时会生成Pb2+Cl2的盐。
【答案】
PbO2?2PbO;Pb2(PbO4);
Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
Pb3O4+8HCl=3PbCl2+Cl2↑+4H2O
精选题
【投影】Fe3O4可以写出Fe2O3?FeO,若把Fe3O4看成是一种盐,又可写成Fe(FeO2)2。根据化合价规律和化学式书写方法,把Pb3O4用上述氧化物形成表示,其化学式为________;若看成是一种盐,化学式为____________。又知,高价Fe不能把HCl氧化,而高价Pb能把HCl氧化成Cl2。试分别写出Fe3O4、Pb3O4与盐酸反应的化学方程式。
引导学生分析,回答:
①铅(Pb)是ⅣA族元素,化合价只有+2价和+4价。根据Fe3O4写成Fe2O3?FeO形式,+4价P:b的氧化物写在前,+2价的氧化物写在后,则有:PbO2?2PbO。
②CuO经H2还原所得的红色产物可能是Cu和Cu2O的混合物。其中不溶于稀H2SO4,但能溶于浓H2SO4、浓HNO3、稀HNO3和FeCl3溶液,其结果都会生成Cu2+;CuO是碱性氧化物,可溶于酸,同时又会发生自身氧化还原反应。
③最后可确定稀H2SO4为鉴定试剂。
【答案】取少量红色产物加入稀H2SO4充分搅拌,如溶液呈蓝色,则证明有Cu2O,反之没有。
即:2Cu+
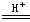 Cu+Cu2+
Cu+Cu2+
给我们提示,应该选择酸溶液为鉴定试剂。
【投影】已知Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。简述如何用最简便的实验方法来检验CuO经H2还原所得到的红色产物中是否含有碱性氧化物Cu2O。要求只从下列试剂中选择:浓H2SO4、浓HNO3、稀H2SO4、稀HNO3、FeCl3。溶液及pH试纸。
引导学生分析,设计出实验方案。
①首先应理解题目给予的信息:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com