
19.(12分)将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:
(2)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是 、 。
①步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是 。
②步骤Ⅳ中发生反应的离子方程式为: 。
六、(本题包括1小题,共12分)
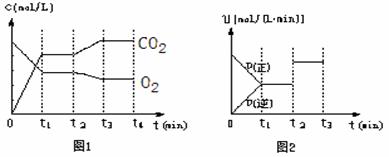
②图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
由图1判断,反应进行至t2 min时,曲线发生变化的原因是 (用文字表达)。由图2判断,t2 min到t3 min 的曲线变化的原因可能是 ____ (填编号)
a.升高温度 b.加了催化剂 c.将原料粉碎 d.缩小容器体积
4FeO?Cr2O3(s)+8Na2CO3(s)+7O2
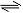 8Na2CrO4(s)+2Fe2O3(s)+8CO2;△H<0
8Na2CrO4(s)+2Fe2O3(s)+8CO2;△H<0
该反应的化学平衡常数的表达式为 。
①步骤I中反应的化学方程式为:
18.(10分)红矾钠(重铬酸钠:Na2Cr2O7?2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
(1) 实验室中红矾钠可用铬铁矿(主要成分:FeO?Cr2O3)利用以下过程来制取。
(4)在100mL0.1mol?L-1E溶液中,逐滴加入35mL 2mol?L-1NaOH溶液,最终得到沉淀物质的量为 。
五、(本题包括1小题,共10分)
17.(10分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
阳离子
H+、Na+、A13+、Ag+、Ba2+
阴离子
OH―、C1―、CO32―、NO3―、SO4―
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(2)写出E溶液与过量的B溶液反应的离子方程式。
。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);
△H=-a KJ?mol-1。请写出B与C的稀溶液反应的热化学方程式
。
请填写下列空白:
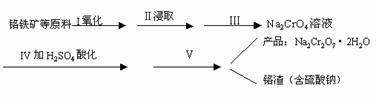
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为 。
(2)从D溶液制备D的无水晶体的“操作a”为 。
(3)反应②的化学方程式为 。
(4)反应⑤的化学方程式为 。
16.(8分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com