
2.将绿矾晶体加强热,除生成水蒸气以外,还发生如下反应:2FeSO4 Fe2O3+SO2↑+SO3↑,如将生成的混和气体通过氯化钡溶液,应发生的现象有
( )
Fe2O3+SO2↑+SO3↑,如将生成的混和气体通过氯化钡溶液,应发生的现象有
( )
A.不一定产生BaSO4沉淀 B.一定产生BaSO3沉淀
C.一定有SO2逸出 D.一定有SO3气体逸出
1.下列氢化物的还原性按由强到弱的顺序排列的是 ( )
A.H2Se>H2S>HI>HBr>HCl B.H2S>H2Se>HI>HBr>HCl
C.HI>HBr>HCl>H2S>H2Se D.H2Se>H2S>HCl>HBr>HI
5.还原法:C+H2O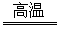 CO+H2,Zn+2HCl=ZnCl2+H2↑
CO+H2,Zn+2HCl=ZnCl2+H2↑
2C+ SiO2 Si+2CO↑
Si+2CO↑
[典型例题]
例1.BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验,它是锗酸铋的简称,若知:①在BGO中,锗处于其最高价态。②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,在此氯化物中铋具有最外层8个电子稳定结构。③BGO可看成是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物所含氧的总质量相同。请填空:
(1)锗和铋的元素符号分别是____、____。
(2)BGO晶体的化学式是____。
(3)BGO晶体所含铋氧化物的化学式是____。
例2.由短周期元素形成的四种常见的非金属单质A、B、C、D。在室温下,它们之中有三种气体,一种固体。在这些单质中,B的式量最小,C次之。这些单质和甲、乙、丙、X、Y五种化合物之间存在如下关系:
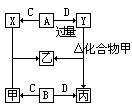
(1)写出化合物乙的化学式______。
(2)上述图示的化学反应共有。种基本反应类型,其中化合反应有______个。
(3)上述四种单质中存在同素异形体的元素是(写元素符号)______。
例3. 有A、B、C、D四种单质。在一定条件下,B可以和A、C、D化合生成化合物甲、乙、丙,C和D化合生成化合物丁。已知甲、乙、丙每个分子中都含有10个电子,并且甲、乙、丙、丁有如下关系:

回答:
(1)单质B的化学式。
(2)单质A与化合物乙反应的化学方程式。
(3)根据化合物丙、丁中D元素化合价判断丙、丁是否在一定条件下生成单质D,简述判断理由。
[课堂练习]
4.氧化法:如MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
4NaBr+3H2SO4+MnO2=2Na2SO4+MnSO4+2Br2+3H2O
2H2S+SO2=3S+2H2O
3.置换法:如Cl2+2NaBr=2NaCl+Br2 2H2S+O2(不足) 2H2O+2S
2H2O+2S
2.分解法:如2KClO3 2KCl+3O2↑
2KCl+3O2↑
CH4 C+2H2 2H2O2
C+2H2 2H2O2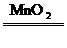 2H2O+O2↑
2H2O+O2↑
1.电解法
①电解水溶液:如2NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
②电解熔融物:如2KHF2 F2↑+H2↑+2KF
F2↑+H2↑+2KF
(1)常见的含氧酸
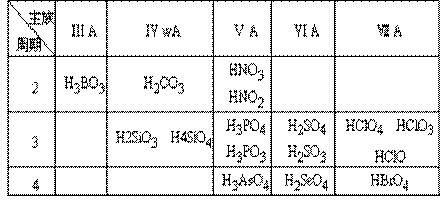
(2)酸性强弱递变规律
同主族由上至下酸性逐渐减弱;同周期由左到右酸性逐渐增强;同种元素中,高价态酸的酸性一般大于低价态酸的酸性。
(3)氧化性酸与还原性酸
常见的强氧化性酸有:HNO3、浓H2SO4、HClO等。
常见的还原性酸有:H2SO3、H3PO3等。
HNO2既有氧化性,又有还原性,但以氧化性为主。
(4)某些酸的特殊性质
浓H2SO4:吸水性→做干燥剂;脱水性→使晶体脱结晶水,使有机物碳化。
HClO:漂白作用。漂白原理与Na2O2同,是利用强氧化性破坏有色物质。
H2SO3:漂白作用。与某些有色物质结合生成不稳定的无色物质,加热后恢复原色。
HF:与SiO2反应。SiO2+4HF→SiF4↑+2H2O
注意:酸的氧化性与氧化性酸是两个不同的概念。酸的氧化性就是指酸中H+结合电子的性质,凡酸皆有此性质。而氧化性酸是指含氧酸的中心元素结合电子的性质。
3.水溶液酸性还原性:非金属元素的非金属性越强,其气态氢化物的还原性越弱;非金属元素的非金属性越弱,其气态氢化物的还原性越强。
2.水溶液酸碱性:ⅥA、ⅦA族元素的气态氢化物的水溶液一般为挥发性酸(HCl、HBr、HI为强酸,其余为弱酸);NH3水溶液碱性,其余不溶,可视为中性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com