
8.“ ”是“关于x的方程
”是“关于x的方程 至少有一个负根”的
( )
至少有一个负根”的
( )
A.充分不必要条件 B.必要不充分条件
C.充要条件 D.既不充分也不必要条件
7.设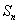 为数列
为数列 的前
的前 项和,
项和, ,则
,则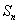 取最小值时,
取最小值时, 的值为 ( )
的值为 ( )
A.12 B.13 C.24 D.25
6.若函数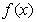 的唯一一个零点同时在区间(0,16),(0,8),(0,4),(0,2)内,则下列结论中正确的是
( )
的唯一一个零点同时在区间(0,16),(0,8),(0,4),(0,2)内,则下列结论中正确的是
( )
A.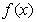 在区间(0,1)内一定有零点
B.
在区间(0,1)内一定有零点
B.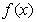 在区间
在区间 内没有零点
内没有零点
C.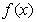 在区间(0,1)或(1,2)内一定有零点
D.
在区间(0,1)或(1,2)内一定有零点
D.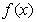 在区间(1,16)内没有零点
在区间(1,16)内没有零点
5.设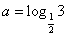 ,
, ,
, ,则
( )
,则
( )
A. B.
B. C.
C. D.
D.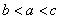
4.已知函数 ,则 (
)
,则 (
)
A. =
= B.
B. =
=
C. =
= D.
D. =
=
3. 设全集 是实数集
是实数集 ,
, 与
与 都是
都是 的子集(如下图所
的子集(如下图所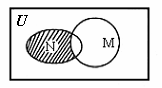 示),
示),
则阴影部分所表示的集合为( )
A. B.
B. 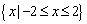
C.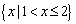 D.
D.
2.函数 的定义域为
( )
的定义域为
( )
A. B.
B. C.
C.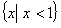 D.
D.
1.下列四个命题中,全称命题是 ( )
A.有些实数是无理数 B.至少有一个整数不能被3整除
C.任意一个偶函数的图象都关于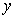 轴对称 D.存在一个三角形不是直角三角形
轴对称 D.存在一个三角形不是直角三角形
12.已知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4。三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某化学兴趣小组通过实验来探究某红色粉末是Fe2O3或Cu2O或两者的混合物。(实验所需试剂只能从下列中选择:稀硫酸、KSCN溶液、稀硝酸、双氧水、铁粉、碱式碳酸铜)
探究方案:将红色粉末溶于足量的稀硫酸中;实验现象:反应后有红色固体存在;
(1)结论:红色粉末是 。
(2)如果红色粉末是Fe2O3和Cu2O的混合物,请设计实验证明之。
实验方法:
实验现象:
(3)兴趣小组欲利用Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知:在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀的pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全的pH |
13 |
14 |
3.7 |
实验小组设计如下实验方案:
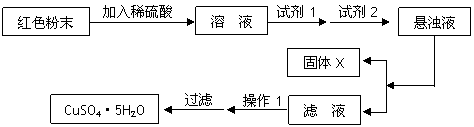
试回答:
①试剂1为 ,试剂2为 (填名称);
②固体X的化学式为 ;
③操作1为 。
答案(1)Cu2O或Fe2O3和Cu2O的混合物;
(2)取少许红色粉末溶于足量稀硫酸中,充分溶解后滴加KSCN溶液,再滴加双氧水;
有红色固体生成,加KSCN溶液不显红色,再加双氧水后显红色。
(3)①双氧水、碱式碳酸铜;②Fe(OH)3;③蒸发、浓缩、冷却、结晶。
11.氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1)配平离子方程式: MnO4-+ HSO3-+ H+-- Mn2++ SO42-+ H2O
(2)滴定过程中,NaHSO3溶液的体积是20.00mL,消耗0.100mol/L的酸性KMnO4溶液16.00mL,则NaHSO3溶液的物质的量浓度是 mol/L。
(3)下列操作会导致测定结果偏高的是
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.滴定前锥形瓶未干燥
C.滴定前滴定管尖嘴部分有气泡
D.不小心将少量酸性KMnO4溶液滴在锥形瓶外
E.观察读数时,滴定前仰视,滴定后俯视
答案.(1)2、5、1、2、5、3 (2)0.2000;(3)ACD
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com