
下图中a、b 为太阳高度日变化曲线。回答3-5题
3.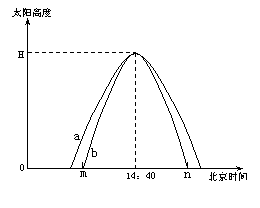 若m为北京时间8:40,且a、b两条曲线分别为Q、
若m为北京时间8:40,且a、b两条曲线分别为Q、
P两地某日太阳高度日变化情况。则
A.Q地昼长小于12小时
B.P地该日正午旗杆影长为零
C.Q地一定位于北半球
D.P地一年中有两次太阳直射
4.若a、b两曲线分别为X、Y两地某日太阳高度
日变化情况。则
A.X、Y两地纬度值相同 B.X、Y两地昼长相同
C.X、Y两地处在同一经线上 D.X、Y两地太阳高度相同
5.若a、b两曲线分别为Z地一年内两天的太阳高度日变化情况。则
A.Z地有极昼极夜现象 B.Z地位于五带中的北温带
C.Z地可能位于拉丁美洲 D.Z地可能位于印度
影刚好投影在地球表面,并且自西向东扫过我国的长江流域,形成日全食观察带(如下图)。届时位于月影区的人们能够观测到日全食。读图回答1-2题

1.月影带自东向西移动的原因是
A.地球自西向东自转 B.地球自西向东公转
C.月球自西向东自转 D.月球自西向东公转
2.成都与重庆日全食的相关描述正确的是
A.成都开始晚、持续时间长 B.成都开始早、持续时间短
C.重庆结束早、持续时间长 D.重庆结束晚、持续时间短
2009年7月22日我国将出现罕见的日全食天象,日、月、地三者位于同一直线,月
18、(2006 山东聊城)25℃时0.1mol·L-1的醋酸溶液的pH约为3,当向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,c(OH-)增大了,因而溶液的pH增大;同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)上述两种解释中 (填“甲”或“乙”)正确
(2) 为了验证上述解释哪种解释正确,继续做如下实验:向0.1mol·L-1的醋酸溶液中加入少量下列物质中的 (填写编号),然后测定溶液的pH
A、固体CH3COOK B、固体CH3CONH4 C、气体NH3 D、固体NaHCO3
(3)若 (填“甲”或“乙”)的解释正确,溶液的pH应 (填“增大”“减小”或“不变”)。(已知25℃时,CH3COONH4溶液呈中性)
(4)常温下将0.010molCH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液。判断:①溶液中共有 种粒子
②其中有两种粒子的物质的量之和一定等于0.010mol,它们是 和
③溶液中n(CH3COO-)+ n(OH-)- n(H+) = mol
17、已知某溶液中存在OH-、H+、NH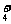 、Cl-四种离子,某同学推测该溶液中离子浓度大小顺序可能有如下四种关系:
、Cl-四种离子,某同学推测该溶液中离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH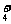 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
②c(Cl-)>c(NH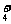 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c(NH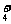 )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)> c(H+)>c(NH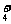 )>c(OH-)
)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) ;(2)若上述关系中③是正确的,则溶液中溶质的化学式是 ;(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“大于”“小于”“等于”下同) c(NH3·H2O),混合前盐酸中c(H+)和氨水中c(OH-)的关系c(H+) c(OH-)
16.(08全国Ⅰ卷)已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1mol/L的NaA和NaB混合溶液中,下列排序正确的是 ( )
A.c(OH)>c(HA)>c(HB)>c(H+) B. c(OH-)>c(A-)>c(B-)>c(H+)
C. c(OH-)>c(B-)>c(A-)>c(H+) D. c(OH-)>c(HB)>c(HA)>c(H+)
15.将7g铁粉加入200 mL 2 mol·L-1的硝酸溶液中,使之充分反应放出NO气体,所得溶
液中主要离子浓度的关系是 ( )
A.c(NO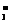 )>c(Fe2+)>c(Fe3+)>c(H+)
)>c(Fe2+)>c(Fe3+)>c(H+)
B.c(NO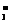 )>c(Fe3+)>c(Fe2+)>c(H+)
)>c(Fe3+)>c(Fe2+)>c(H+)
C.c(Fe2+)>c(Fe3+)>c(NO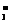 )>c(H+)
)>c(H+)
D.2c(Fe2+)+3c(Fe3+)+c(H+)═c(NO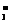 )+c(OH-)
)+c(OH-)
14.下列关于电解质溶液中离子关系的说法中正确的是 ( )
A.0.1mol·L-1Na2C03溶液中离子浓度关系:
c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3)
B.0.1mol·L-1NH4C1和0.1mol·L-1NH3·H20等体积混合后离子浓度关系:
c(Cl-)>c(NH+ 4)>c(H+)>c(OH-)
C.常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:
c(Na+)=c(CH3COO-)
D.常温下,在pH=1的溶液中,Fe2+、NO3-、C1O-、Na+能大量共存
13.将0.2摩/升CH3COONa与0.1摩/升盐酸等体积混和后,溶液中下列微粒的物质的量浓度的关系正确的是(盐和酸混和液) ( )
A.[CH3COO-]=[Cl-]=[H+]>[CH3COOH]
B.[CH3COO-]=[Cl-]>[CH3COOH]>[H+]
C.[CH3COO-]>[Cl-]>[H+]>[CH3COOH]
D.[CH3COO-]>[Cl-]>[CH3COOH]>[H+]
12.在Na2S水溶液中,下列关系不正确的是 (二元弱酸正盐) ( )
A.[OH-] = [HS-] + [H+] + [H2S] B.[Na+] + [H+] = [OH-] + 2[S2-] + [HS-]
C.[OH-] = [ HS-] + [H+] + 2[H2S] D.[Na+] = 2[S2-] + 2[ HS-] + 2[H2S]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com