
2.反应2A(气) 2B(气)+C(气);ΔΗ> 0,在未用催化剂的条件下已达到平衡,现要使正反应速率降低,[B]减小,应采用的措施……… …………………
(
)
2B(气)+C(气);ΔΗ> 0,在未用催化剂的条件下已达到平衡,现要使正反应速率降低,[B]减小,应采用的措施……… …………………
(
)
A、升温 B、增大反应器体积 C、增大[A] D、降温
1.在恒温、恒容的密闭容器进行反应A(g) B(g)+C(g);ΔΗ> 0。若反应物的浓度由2mol/L降到0.8mol/L需要20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需要反应时间为……………………………………………………
…
(
)
B(g)+C(g);ΔΗ> 0。若反应物的浓度由2mol/L降到0.8mol/L需要20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需要反应时间为……………………………………………………
…
(
)
A、10 s B、大于10s C、小于10s D、无法判断
5、NO和CO都是汽车尾气里有害的物质,它们能缓慢地起反应生成N2和CO2,对此反应,下列叙述中正确的是…………………………………………………… ( )
A、使用催化剂不能改变反应速率 B、降低压强能使反应速率加快
C、改变压强对反应速率没有影响 D、升高温度能加快反应速率
课外作业
4、在2SO2(气)+O2(气) 2SO3(气)反应中,反应物消耗速率、生成物的生成速率之间的关系不正确的是………………………………………
(
)
2SO3(气)反应中,反应物消耗速率、生成物的生成速率之间的关系不正确的是………………………………………
(
)
 A、V(SO2)=V(O2)=V(SO3) B、V(O2)=1/2
V(SO2)
A、V(SO2)=V(O2)=V(SO3) B、V(O2)=1/2
V(SO2)
C、V(SO2)= V(SO3) D、V(SO3)= 2V(O2)
3、可逆反应2SO2 + O2  2SO3,如果SO2的起始浓度为2 mol/L ,2min后SO2的浓度为1.8mol/L,则用SO2的浓度变化表示的反应速率为…………………
(
)
2SO3,如果SO2的起始浓度为2 mol/L ,2min后SO2的浓度为1.8mol/L,则用SO2的浓度变化表示的反应速率为…………………
(
)
A、1mol/(L·min) B、0.9mol/(L·min)
C、0.2mol/(L·min) D、0.1mol/(L·min)
2、设反应C + CO2  2CO ΔΗ1> 0反应速率为V1
;N2 + 3H2 == 2NH3ΔΗ2< 0 ,反应速率为V2
。对上述反应,当温度升高时,V1和V2的变化为…………… ( )
2CO ΔΗ1> 0反应速率为V1
;N2 + 3H2 == 2NH3ΔΗ2< 0 ,反应速率为V2
。对上述反应,当温度升高时,V1和V2的变化为…………… ( )
A、同时增大 B、同时减小
C、V1增大,V2减少 D、V1减小,V2增大
1、 用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是 ( )
A、对该反应体系加热 B、不能稀硫酸,改用98%的浓硫酸
C、滴加少量CuSO4溶液 D、不用铁片,改用铁粉
2、可逆反应A(气)+2B(气) nC(气),在不同压强(P1、P2)下,测得C的体积分数跟反应时间的关系如图所示,以下结论正确的是…………………( )
nC(气),在不同压强(P1、P2)下,测得C的体积分数跟反应时间的关系如图所示,以下结论正确的是…………………( )
 A、P1>P2 ,n >3 B、P1>P2 ,n <3
A、P1>P2 ,n >3 B、P1>P2 ,n <3
C、P1<P2 ,n >3 D、P1<P2 ,n <3
思维方法: 。
展望高考:
[巩固练习]
课堂反馈
1、在密闭容器中充入A、B或G、H进行可逆反应:aA(气)+bA(气) gG(气)+hH(气);△H=QkJ/mol ,图甲、图乙分别表示在虚线所示部位改变温度(T)或压强对化学平衡与反应速率的影响(t表示时间),则下列结论中正确的是…………………………………( )
gG(气)+hH(气);△H=QkJ/mol ,图甲、图乙分别表示在虚线所示部位改变温度(T)或压强对化学平衡与反应速率的影响(t表示时间),则下列结论中正确的是…………………………………( )
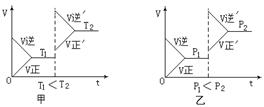
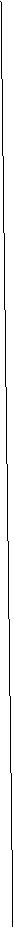
A、开始时充入G和H a+b<g+h Q<0
B、开始时充入G和H a+b<g+h Q>0
C、开始时充入G和H a+b>g+h Q>0
D、开始时充入A和B a+b>g+h Q>0
思维方法: 。
展望高考:
3.外界条件对反应速率的影响是由 决定的;
 (1)浓度的影响就是
(1)浓度的影响就是
(2)压强的影响就是 ;
(3)温度的影响就是
(4)催化剂的影响就是
[小结]外界条件对化学反应速率影响的规律(勒沙特列原理)
。
[例题解析]
[例1]在2A + B 3C + 4D反应中,表示该反应速率最快的是( )
3C + 4D反应中,表示该反应速率最快的是( )
A VA = 0.5 mol·L-1·S-1 B VB = 0.3 mol ·L-1·S-1
C VC = 0.8 mol·L-1·S-1
D VD= 1 mol L-1·S-1
解题思路: 。
易错点: 。
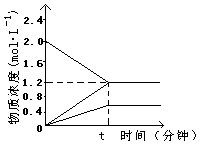
[例2] 右图表示800℃ 时A、B、C三种气体物质的浓度随时间变化的情况,t
是到达平衡状态的时间。试回答:
(1) 该反应的反应物是_____________。
(2) 该反应的化学反应方程式为_____________。
(3) 若达到平衡状态的时间是2分钟,A物质的平均反应速率为___________。
解题思路: 。
易错点: 。
[考题再现]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com