
15.在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol/L的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是( )

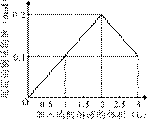
A B

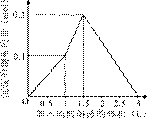
C D
14.将干燥锌粉和碘粉混合,未发生明显变化,而滴加数滴水后,立即产生紫色气体。由此可得出正确结论的是( )。
A.水与碘反应放出大量的热使碘升华 B. 没有发生化学变化,只有物理变化
C.锌和碘化合生成碘化锌是放热反应 D. 以上说法都不正确
13.下列各组离子在溶液中按一定的物质的量之比(见括号)混合,所得溶液为无色透明,且pH>7的是( )
A.Al3+、Cl-、Na+、CO32- (1∶3∶2∶1) B.HCO3-、K+、H+、I- (1∶1∶1∶1)
C.Ca2+、K+、OH-、HCO3- (1∶1∶1∶2) D.NH4+、Ba2+、OH-、Cl- (2∶1∶2∶2)
12.下列各项实验操作中,正确的是 ( )
A.为使制取H2的速率加快,可向H2SO4中加少量CuSO4溶液
B.为加快过滤速度,可用玻璃棒搅拌过滤器中的食盐水
C.配制一定物质的量浓度的溶液时,容量瓶用水洗涤后再用所配溶液洗涤
D.为除去试管内壁上的“银镜”,可用氨水洗涤
11.下列各组溶液,不用其他试剂就不能鉴别的是( )
A.AgNO3、KNO3、KCl、NaI B.NaOH、MgSO4、Na2CO3、NaHSO4
C.FeCl3、NaNO3、Na2CO3、NaCl D.HCl、BaCl2、NaOH、CuSO4
10.能大量共存于同一溶液中,且当水电离出的c(H+)=10-13 mol·L-1时,又能发生反应的离子组是( )①Na+、Ba2+、C1-、HCO3- ②K+、NH4+、CH3COO-、SO42-
③Ca2+、NH4+、SO42-、SO32- ④Fe3+、Na+、SCN-、C1- ⑤A13+、Na+、HCO3-、NO3-
A.只有① B.②③ C.①② D.①④
9.浓度为2mol/L的氢溴酸溶液VL,欲使其浓度变为4mol/L,以下列出的方法中可行的是( )
A.通入标况下的HBr气体44.8L B.将溶液加热蒸发浓缩至0.5V
C.蒸发掉0.5L水 D.加入10mol/L氢溴酸0.6VL,再将溶液稀释至2VL
8.氯酸是一种强酸,浓度超过40%时会发生分解反应可表示为:
aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法不正确的是( )
A.该反应既是分解反应,又是氧化还原反应
B.变蓝的淀粉碘化钾试纸褪色可能发生的反应:
5C12+I2+6H2O=12H++10Cl-+2IO3-
C.若化学计量数a=8,b=3,则该反应转移电子数为20e-
D.氯酸分解所得O2和Cl2的物质的量之比是确定不变的
7.碘化钾可跟氯气反应置换出碘,而碘又能与氯酸钠反应置换出氯气,两反应式为:2KI+Cl2→2KCl+I2 2NaClO3+I2→2NaIO3+Cl2
对上述两实际发生的反应的正确叙述是( )
A.在个别反应中碘的非金属性比氯强 B.在个别反应中碘的氧化性强于氯气
C.碘酸钠的氧化性比氯酸钠强 D.氯气的氧化性均比碘强
6.用铝箔包装0.1mol金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为(标准状况)( )
A.O2和H2的混合气体 B.大于1.12 L H2
C.1.12 L H2 D.小于1.12 L H2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com