
14.当夜半球与“陆半球”重叠最多时:
A.非洲全部位于昼半球
B.北京市正值下班高峰
C.南极昆仑站处于极昼期
D.江苏各地太阳高度达一年中最大值
13.“水半球”的极点位于:
A.北半球、东半球 B.北半球、西半球
C.南半球、东半球 D.南半球、西半球
2006年7月1日,青藏铁路全线通车开始运行。2008年8月8日20时,第二十九届奥运会开幕式在北京国家体育场(鸟巢)隆重举行。“同一个世界、同一个梦想”(One world、One dream)成为北京奥运会中英文主题口号。读图完成11-12题。
11.图1中北京奥运会吉祥物“福娃”代表的珍稀动物生活在青藏铁路沿线的是:

12.下图中最能表现青藏铁路经过地区咸水湖的是:

A.① B.② C.③ D.④
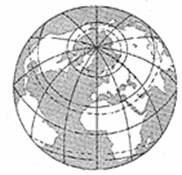 图2所示为以38°N、0°为极点的陆地相对集中的“陆半球”(另一半
图2所示为以38°N、0°为极点的陆地相对集中的“陆半球”(另一半 球为“水半球”)。读图回答13-14题。
球为“水半球”)。读图回答13-14题。
下图中,大圆为晨昏线,M点纬度为70°,且该点位于东、西半球的分界线上,P点线速度为0,图中阴影区与非阴影区的日期不同。读图回答9-10题。
9.若图中日期为3日和4日,则北京时间为:
 A.3日2时40分
A.3日2时40分
B.3日21时20分
C.4日2时40分
D.4日21时20分
10.有一架飞机准备从Q点起飞,沿图中虚线
示意路线飞行,至M点降落,则:
A.飞机飞行方向保持不变
B.飞行中一直阳光普照
C.航线是QM两地间最近距离
D.飞机将飞越太平洋上空
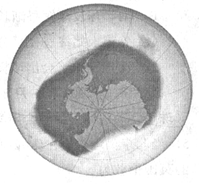 读右图完成7-8题。
读右图完成7-8题。
7.图示臭氧空洞(空中阴影区域)出现在:
A.北极地区 B.青藏高原
C.南极地区 D.墨西哥湾
8.地球大气层的臭氧:
A.集中分布的高度为17-18千米
B.能大量吸收太阳辐射中的可见光
C.损耗严重是由于CO2的含量过高
D.减少会使到达地面的紫外线增强
读地球绕太阳公转示意图(图2),完成5-6题。
5.图中显示12月22目前后地球在公转轨道上的位置为:
 A.Q1
B.Q2
A.Q1
B.Q2
C.Q3 D.Q4
6.当地球由Q1公转到Q2的过程中:
A.北半球昼渐长夜渐短
B.南半球昼渐长夜渐短
C.赤道上早于6点日出
D.南极圈内不会出现极夜
据美国宇航局最新消息,2009年9月21日到9月30日地球大气层臭氧损耗严重。据此
北京时间2009年3月1日16时13分10秒嫦娥一号撞击月面,据此回答3-4题。
3.撞击时,地球上可能出现的地理现象是:
A.太阳直射点南移 B.赤道地区昼夜平分
C.北京白昼时间一年中最长 D.南极点附近出现极夜
4.嫦娥一号撞击月球所遗留的痕迹,未来将受到的外力作用是:
A.风化作用 B.流水侵蚀 C.风力搬运 D.岩浆活动
20.(16分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 。其中心原子采
取 杂化。
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 ,
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
永安一中2008-2009学年下学期第一次月考
19、(12分)氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。请回答下列问题。
(1)砷原子核外电子排布式为______________________________。(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为________________,该晶体的配位体为____________。
(3)已知:
|
|
CH4 |
SiH4 |
NH3 |
PH3 |
|
沸点(K) |
101.7 |
161.2 |
239.7 |
185.4 |
|
分解温度(K) |
873 |
773 |
1073 |
713.2 |
分析上表中四种物质的相关数据,请回答:
① CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是_____________________________。
② CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是_________________________。
③综合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时__________先液化。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com