
(13)ШєКЏЪ§ дђ
дђ ___________.
___________.
(14)КЏЪ§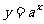 дк[0,1]ЩЯЕФзюДѓжЕгызюаЁжЕЕФКЭЮЊ3ЃЌдђaЃНЁЁЁЁЁЁ
дк[0,1]ЩЯЕФзюДѓжЕгызюаЁжЕЕФКЭЮЊ3ЃЌдђaЃНЁЁЁЁЁЁ
(15)КЏЪ§ ЖдШЮвтЕФЪЕЪ§
ЖдШЮвтЕФЪЕЪ§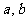 ЖМТњзу:
ЖМТњзу: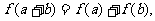 Чв
Чв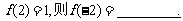
(16)ЖЈвхдк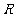 ЩЯЕФХМКЏЪ§
ЩЯЕФХМКЏЪ§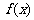 ТњзуЃК
ТњзуЃК ЃЌЧвдк
ЃЌЧвдк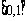 ЩЯЪЧдіКЏЪ§ЃЌЯТУцЙигк
ЩЯЪЧдіКЏЪ§ЃЌЯТУцЙигк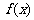 ЕФХаЖЯЃКЂй
ЕФХаЖЯЃКЂй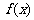 ЪЧжмЦкКЏЪ§ЃЛЂк
ЪЧжмЦкКЏЪ§ЃЛЂк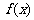 ЕФЭМЯѓЙигкжБЯп
ЕФЭМЯѓЙигкжБЯп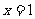 ЖдГЦЃЛЂл
ЖдГЦЃЛЂл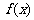 дк
дк ЩЯЪЧМѕКЏЪ§ЃЛЂм
ЩЯЪЧМѕКЏЪ§ЃЛЂм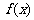 дк
дк ЩЯЪЧМѕКЏЪ§.Цфжае§ШЗЕФХаЖЯЪЧ_____________(АбФуШЯЮЊе§ШЗЕФХаЖЯЖМЬюЩЯ).
ЩЯЪЧМѕКЏЪ§.Цфжае§ШЗЕФХаЖЯЪЧ_____________(АбФуШЯЮЊе§ШЗЕФХаЖЯЖМЬюЩЯ).
(1)ШєМЏКЯ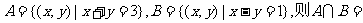

(2)ЬѕМў :ЃќxЃќЃО1ЃЌЬѕМўqЃКxЃМЃ2ЃЌдђpЪЧqЕФ
:ЃќxЃќЃО1ЃЌЬѕМўqЃКxЃМЃ2ЃЌдђpЪЧqЕФ
 БивЊВЛГфЗжЬѕМўЁЁЁЁ
БивЊВЛГфЗжЬѕМўЁЁЁЁ 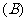 ГфЗжВЛБивЊЬѕМўЁЁ
ГфЗжВЛБивЊЬѕМўЁЁ  ГфвЊЬѕМўЁЁЁЁ
ГфвЊЬѕМўЁЁЁЁ 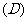 ЗЧГфЗжЗЧБивЊЬѕМў
ЗЧГфЗжЗЧБивЊЬѕМў
(3)вбжЊf(x)= ЃЌ
ЃЌ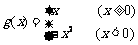 ЃЌдђ
ЃЌдђ
ЁЁ Ѓ4ЁЁЁЁЁЁЁЁЁЁ
Ѓ4ЁЁЁЁЁЁЁЁЁЁ
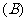 4ЁЁЁЁЁЁЁЁ
ЁЁ
4ЁЁЁЁЁЁЁЁ
ЁЁ  Ѓ2ЁЁЁЁЁЁЁЁ
Ѓ2ЁЁЁЁЁЁЁЁ
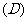 2
2
(4)ЖЈвхМЏКЯAЁЂBЕФвЛжждЫЫуЃКAЃЊBЃН{xЃќxЃНx1+x2ЃЌx1ЁЪAЃЌx2ЁЪB}ЃЌШєAЃН{1,2ЃЌ3}ЃЌЁЁ BЃН{1,2}ЃЌдђAЃЊBжаЕФЫљгадЊЫижЎКЭЮЊ
ЁЁ(A)21ЁЁЁЁЁЁ(B)18ЁЁЁЁЁЁ(C)14ЁЁЁЁЁЁ(D)9
(5)КЏЪ§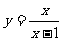 ЕФЭМЯѓЪЧ
ЕФЭМЯѓЪЧ
 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
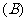 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ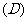 ЁЁ
ЁЁ
(6)КЏЪ§ ЕФЗДКЏЪ§ЪЧ
ЕФЗДКЏЪ§ЪЧ


(7)ЩшШЋМЏЮЊRЃЌA= (aЮЊГЃЪ§)ЃЌЧв11ЁЪBЃЌдђ
(aЮЊГЃЪ§)ЃЌЧв11ЁЪBЃЌдђ
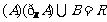 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ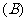


 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ 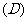

(8)КЏЪ§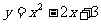 дкЧјМф
дкЧјМф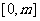 ЩЯгазюДѓжЕ3ЃЌзюаЁжЕ2ЃЌдђ
ЩЯгазюДѓжЕ3ЃЌзюаЁжЕ2ЃЌдђ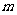 ЕФШЁжЕЗЖЮЇЪЧ
ЕФШЁжЕЗЖЮЇЪЧ

(9)КЏЪ§ ЭМЯѓЕФЖдГЦжсЗНГЬЪЧ
ЭМЯѓЕФЖдГЦжсЗНГЬЪЧ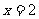 ЃЌФЧУДaЕШгк
ЃЌФЧУДaЕШгк

(10)ЯТСаКЏЪ§жаЃЌЭЌЪБОпгааджЪЃК(1)ЭМЯѓЙ§Еу(0ЃЌ1)ЃЛ(2)дкЧјМф ЩЯЪЧМѕКЏЪ§ЃЛ
ЩЯЪЧМѕКЏЪ§ЃЛ
(3)ЪЧХМКЏЪ§.етбљЕФКЏЪ§ЪЧ

(11)Щш ЪЧЖЈвхдк
ЪЧЖЈвхдк ЩЯЕФКЏЪ§ЃЌЖдгкШЮвт
ЩЯЕФКЏЪ§ЃЌЖдгкШЮвт ЧвЕБ
ЧвЕБ ЪБЃЌ
ЪБЃЌ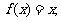 дђ
дђ


(12)гвЭМЫљЪОЕФФГГиЬСжаЕФИЁЦМТћбгЕФУцЛ§ гыЪБМф
гыЪБМф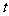 (дТ)ЕФЙиЯЕЮЊЃК
(дТ)ЕФЙиЯЕЮЊЃК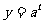 .гавдЯТХаЖЯЃКЂйетИіжИЪ§КЏЪ§ЕФЕзЪ§ЮЊ2ЃЛЂкЕк5ИідТКѓЃЌИЁЦМУцЛ§ОЭЛсГЌЙ§30
.гавдЯТХаЖЯЃКЂйетИіжИЪ§КЏЪ§ЕФЕзЪ§ЮЊ2ЃЛЂкЕк5ИідТКѓЃЌИЁЦМУцЛ§ОЭЛсГЌЙ§30 ЃЛЂлИЁЦМУПдТдіМгЕФУцЛ§ЖМЯрЕШЃЛЂмШєИЁЦМТћбгЕН
ЃЛЂлИЁЦМУПдТдіМгЕФУцЛ§ЖМЯрЕШЃЛЂмШєИЁЦМТћбгЕН ЃЌ
ЃЌ ЫљОЙ§ЕФЪБМфЗжБ№ЮЊ
ЫљОЙ§ЕФЪБМфЗжБ№ЮЊ дђ
дђ .ЦфжаХаЖЯе§ШЗЕФИіЪ§ЪЧ
.ЦфжаХаЖЯе§ШЗЕФИіЪ§ЪЧ

42.(2006ФъНЫеОэ(10Зж))РћгУЬЋбєЙтЗжНтЫЎжЦЧтЪЧЮДРДНтОіФмдДЮЃЛњЕФРэЯыЗНЗЈжЎвЛЁЃФГбаОПаЁзщЩшМЦСЫШчгвЭМЫљЪОЕФбЛЗЯЕЭГЪЕЯжЙтЗжНтЫЎжЦЧтЁЃЗДгІЙ§ГЬжаЫљашЕФЕчФмгЩЬЋбєФмЙтЕчГиЬсЙЉЃЌЗДгІЬхЯЕжаI2КЭFe3+ЕШПЩбЛЗЪЙгУЁЃ
ЂХаДГіЕчНтГиAЁЂЕчНтГиBКЭЙтДпЛЏЗДгІГижаЗДгІЕФРызгЗНГЬЪНЁЃ
ЂЦШєЕчНтГиAжаЩњГЩ3.36 L H2(БъзМзДПі)ЃЌЪдМЦЫуЕчНтГиBжаЩњГЩFe2+ЕФЮяжЪЕФСПЁЃ
ЂЧШєбЛЗЯЕЭГДІгкЮШЖЈЙЄзїзДЬЌЪБЃЌЕчНтГиAжаСїШыКЭСїГіЕФHIХЈЖШЗжБ№ЮЊa molЁЄL-КЭb molЁЄLЃ1ЃЌЙтДпЛЏЗДгІЩњГЩFe3+ЕФЫйТЪЮЊc molЁЄLЃ1ЃЌбЛЗЯЕЭГжаШмвКЕФСїСПЮЊQ(СїСПЮЊЕЅЮЛЪБМфФкСїЙ§ЕФШмвКЬхЛ§)ЁЃЪдгУКЌЫљИјзжФИЕФДњЪ§ЪНБэЪОШмвКЕФСїСПQЁЃ

41. (2006ФъББОЉОэ)(14Зж)ТСКЭЧтбѕЛЏМиЖМЪЧживЊЕФЙЄвЕВњЦЗЁЃЧыЛиД№ЃК
(1)ЙЄвЕвБСЖТСЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(2)ТСгыЧтбѕЛЏМиЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(3)ЙЄвЕЦЗЧтбѕЛЏМиЕФШмвКжаКЌгаФГаЉКЌбѕЫсИљдгжЪЃЌПЩгУРызгНЛЛЛФЄЗЈЕчНтЬсДПЁЃЕчНтВлФкзАгабєРызгНЛЛЛФЄ(жЛдЪаэбєРызгЭЈЙ§)ЃЌЦфЙЄзїдРэШчЭМЫљЪОЁЃ


ЂйИУЕчНтВлЕФбєМЋЗДгІЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЂкЭЈЕчПЊЪМКѓЃЌвѕМЋИННќШмвКpHЛсдіДѓЃЌЧыМђЪідвђЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂЧЂйЁЁ 4OH?? 4e? = 2H2O + O2ЁќЂк H+ЗХЕчЃЌДйНјЫЎЕФЕчРыЃЌOH?ХЈЖШдіДѓЂл B
ЂлГ§ШЅдгжЪКѓЧтбѕЛЏМиШмвКДгвКЬхГіПкЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюаДЁАAЁБЛђЁАBЁБ)ЕМГіЁЃ
40.(2005ФъШЋЙњ)(15Зж)XЁЂYЁЂZЁЂWЮЊАДдзгађЪ§гЩаЁЕНДѓХХСаЕФЫФжжЖЬжмЦкдЊЫиЁЃ
вбжЊЃКЂйXПЩЗжБ№гыYЁЂWаЮГЩX2YЃЌX2Y2ЁЂXWЕШЙВМлЛЏКЯЮяЃЛ
ЂкZПЩЗжБ№гыYЁЂWаЮГЩZ2YЁЂZ2Y2ЁЂZWЕШРызгЛЏКЯЮяЁЃ
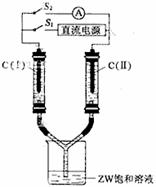 ЧыЛиД№ЃК
ЧыЛиД№ЃК
(1)Z2YЕФЛЏбЇЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)Z2Y2гыX2YЗДгІЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ШчЭМЫљЪОзАжУЃЌСНВЃСЇЙмжаЪЂТњЕЮгаЗгЬЊШмвКЕФZWБЅКЭШмвКЃЌC(Ђё)ЁЂC(Ђђ)ЮЊЖрПзЪЏФЋЕчМЋЁЃ
НгЭЈS1КѓЃЌC(Ђё)ИННќШмвКБфКьЃЌСНВЃСЇЙмжагаЦјЬхЩњГЩЁЃвЛЖЮЪБМфКѓ(СНВЃСЇЙмжавКУцЮДЭбРыЕчМЋ)ЃЌЖЯПЊS1ЃЌНгЭЈS2ЃЌЕчСїБэЕФжИеыЗЂЩњЦЋзЊЁЃДЫЪБЃК
C(I)ЕФЕчМЋУћГЦЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюаДе§МЋЛђИКМЋ)ЃЛ
C(II)ЕФЕчМЋЗДгІЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ЭаМЗХШыЯЁСђЫсВЛЗЂЩњЗДгІЃЌШєдкЯЁСђЫсжаМгШыX2Y2ЃЌЭаМПЩж№НЅШмНтЃЌИУЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁ ЁЃ
39ЃЎ
 (2004ШЋЙњ)дкВЃСЇдВЭВжаЪЂгаСНжжЮоЩЋЕФЛЅВЛЯрШмЕФжаадвКЬхЁЃЩЯВувКЬхжаВхШыСНИљЪЏФЋЕчМЋЃЌдВЭВФкЛЙЗХгавЛИљЯТЖЫЭфГЩЛЗзДЕФВЃСЇНСАєЃЌПЩвдЩЯЯТНСЖЏвКЬхЃЌзАжУШчгвЭМЁЃНгЭЈЕчдДЃЌбєМЋжмЮЇЕФвКЬхГЪЯжзиЩЋЃЌЧвбеЩЋгЩЧГБфЩюЃЌвѕМЋЩЯгаЦјХнЩњГЩЁЃЭЃжЙЭЈЕчЃЌШЁГіЕчМЋЃЌгУНСАєЩЯЯТОчСвНСЖЏЁЃОВжУКѓвКЬхгжЗжГЩСНВуЃЌЯТВувКЬхГЪзЯКьЩЋЃЌЩЯВувКЬхМИКѕЮоЩЋЁЃИљОнЩЯЪіЪЕбщЛиД№ЃК
(2004ШЋЙњ)дкВЃСЇдВЭВжаЪЂгаСНжжЮоЩЋЕФЛЅВЛЯрШмЕФжаадвКЬхЁЃЩЯВувКЬхжаВхШыСНИљЪЏФЋЕчМЋЃЌдВЭВФкЛЙЗХгавЛИљЯТЖЫЭфГЩЛЗзДЕФВЃСЇНСАєЃЌПЩвдЩЯЯТНСЖЏвКЬхЃЌзАжУШчгвЭМЁЃНгЭЈЕчдДЃЌбєМЋжмЮЇЕФвКЬхГЪЯжзиЩЋЃЌЧвбеЩЋгЩЧГБфЩюЃЌвѕМЋЩЯгаЦјХнЩњГЩЁЃЭЃжЙЭЈЕчЃЌШЁГіЕчМЋЃЌгУНСАєЩЯЯТОчСвНСЖЏЁЃОВжУКѓвКЬхгжЗжГЩСНВуЃЌЯТВувКЬхГЪзЯКьЩЋЃЌЩЯВувКЬхМИКѕЮоЩЋЁЃИљОнЩЯЪіЪЕбщЛиД№ЃК
(1)бєМЋЩЯЕФЕчМЋЗДгІЪНЮЊ_____________________ЁЃ
(2)вѕМЋЩЯЕФЕчМЋЗДгІЪНЮЊ_____________________ЁЃ
(3)дЩЯВувКЬхЪЧ_____________________________ЁЃ
(4)дЯТВувКЬхЪЧ______________________________ЁЃ
(5)НСАшКѓСНВувКЬхбеЩЋЗЂЩњБфЛЏЕФдвђЪЧ________
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(6)вЊМьбщЩЯВувКЬхжаКЌгаЕФН№ЪєРызгЃЌЦфЗНЗЈЪЧ______________ЃЌ
ЁЁЁЁ ЯжЯѓЪЧ_______________________________ЁЁ
_____________ЁЃ
38ЃЎ(08КЃФЯОэ)ШчКЮЗРжЙЬњЕФатЪДЪЧЙЄвЕЩЯбаОПЕФжиЕуФкШнЁЃЮЊбаОПЬњатЪДЕФгАЯьвђЫиЃЌФГЭЌбЇзіСЫШчЯТЬНОПЪЕбщЃК
|
ађКХ |
ФкШн |
ЪЕбщЯжЯѓ |
|
1 |
ГЃЮТЯТНЋЬњЫПЗХдкИЩдяПеЦјжавЛИідТ |
ИЩдяЕФЬњЫПБэУцвРШЛЙтСС |
|
2 |
ГЃЮТЯТНЋЬњЫПЗХдкГБЪЊПеЦјжавЛаЁЪБЁЁ |
ЬњЫПБэУцвРШЛЙтССЁЁ |
|
3 |
ГЃЮТЯТНЋЬњЫПЗХдкГБЪЊЕФПеЦјжавЛИідТ |
ЬњЫПБэУцвбБфЕУЛвАЕ |
|
4 |
НЋГБЪЊЕФЬњЫПЗХдкГЃЮТЕФбѕЦјСїжавЛаЁЪБ |
ЬњЫПБэУцТдЯдЛвАЕ |
|
5 |
НЋГБЪЊЕФЬњЫПЗХдкИпгкГЃЮТЕФбѕЦјСїжавЛаЁЪБ |
ЬњЫПБэУцвбБфЕУЛвАЕ |
|
6 |
НЋНўЙ§ТШЛЏФЦШмвКЕФЬњЫПЗХдкИпгкГЃЮТЕФбѕЦјСїжавЛаЁЪБ |
ЬњЫПБэУцЛвАЕГЬЖШБШЪЕбщ5бЯжи |
ЛиД№вдЯТЮЪЬтЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(1)ЩЯЪіЪЕбщжаЗЂЩњСЫЕчЛЏбЇИЏЪДЕФЪЧ(ЬюЪЕбщађКХ) __________; дкЕчЛЏбЇИЏЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЪДжаЃЌИКМЋЗДгІЪЧ________________; е§МЋЗДгІЪЧ_______________________ЃЛЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)гЩИУЪЕбщПЩжЊЃЌПЩвдгАЯьЬњатЪДЫйТЪЕФвђЫиЪЧ___________________________ЃЛЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(3)ЮЊЗРжЙЬњЕФатЪДЃЌЙЄвЕЩЯЦеБщВЩгУЕФЗНЗЈЪЧ______________(Д№СНжжЗНЗЈ)ЁЁ
37ЃЎ(08ББОЉОэ)ОнБЈЕРЃЌЮвЙњгЕгаЭъШЋзджїВњШЈЕФЧтбѕШМСЯЕчГиГЕНЋдкАТдЫЛсЦкМфЮЊдЫЖЏдБЬсЙЉЗўЮёЁЃФГжжЧтбѕШМСЯЕчГиЕФЕчНтвКЮЊKOHШмвКЁЃЯТСагаЙиЕчГиЕФа№ЪіВЛе§ШЗЕФЪЧ(ЁЁ )
AЃЎе§МЋЗДгІЪНЮЊЃКO2+2H2O+4eЃ ===4OHЃ
BЃЎЙЄзївЛЖЮЪБМфКѓЃЌЕчНтвКжаЕФKOHЕФЮяжЪЕФСПВЛБф
CЃЎИУШМСЯЕчГиЕФзмЗДгІЗНГЬЪНЮЊЃК2H2+O2===2H2O
DЃЎгУИУЕчГиЕчНтCuCl2ШмвКЃЌВњЩњ2.24LCl2(БъзМзДПі)ЪБЃЌга0.1molЕчзгзЊвЦ
36ЃЎ(08ЬьНђОэ)ЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎдкдЕчГиЕФИКМЋКЭЕчНтГиЕФвѕМЋЩЯЖМЪЧЗЂЩњЪЇЕчзгЕФбѕЛЏЗДгІ
BЃЎгУЖшадЕчМЋЕчНтNa2SO4ШмвКЃЌвѕбєСНМЋВњЮяЕФЮяжЪЕФСПжЎБШЮЊ1ЃК2
CЃЎгУЖшадЕчМЋЕчНтБЅКЭNaClШмвКЃЌШєга1 molЕчзгзЊвЦЃЌдђЩњГЩ1 molNaOH
DЃЎЖЦВуЦЦЫ№КѓЃЌЖЦЮ§ЬњАхБШЖЦаПЬњАхИќФЭИЏЪД
35ЃЎ (08ЙуЖЋОэ)ЕчГиЪЧШЫРрЩњВњКЭЩњЛюжаЕФживЊФмСПРДдДЃЌИїЪНИїбљЕчГиЕФЗЂеЙЪЧЛЏбЇЖдШЫРрЕФвЛЯюжиДѓЙБЯзЁЃЯТСагаЙиЕчГиЕФа№Ъіе§ШЗЕФЪЧ(ЁЁ )
(08ЙуЖЋОэ)ЕчГиЪЧШЫРрЩњВњКЭЩњЛюжаЕФживЊФмСПРДдДЃЌИїЪНИїбљЕчГиЕФЗЂеЙЪЧЛЏбЇЖдШЫРрЕФвЛЯюжиДѓЙБЯзЁЃЯТСагаЙиЕчГиЕФа№Ъіе§ШЗЕФЪЧ(ЁЁ )
AЃЎаПУЬИЩЕчГиЙЄзївЛЖЮЪБМфКѓЬМАєБфЯИ
BЃЎЧтбѕШМСЯЕчГиПЩНЋШШФмжБНгзЊБфЮЊЕчФм
CЃЎЧтбѕШМСЯЕчГиЙЄзїЪБЧтЦјдкИКМЋБЛбѕЛЏ
DЃЎЬЋбєФмЕчГиЕФжївЊВФСЯЪЧИпДПЖШЕФЖўбѕЛЏЙш
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com