
3.定量MnO2与VmL10mol/L的盐酸共热制氯气,标准状况下产生2.24L氯气,则V的取值应为 ( )
A . V=20 B . 20<V<40 C. V=40 D. V>40
2. 10mL0.8mol/LMn+的溶液,恰好能沉淀30mL0.4mol/LCO2-3的溶液,则n为
10mL0.8mol/LMn+的溶液,恰好能沉淀30mL0.4mol/LCO2-3的溶液,则n为
( )
A. 1 B. 2 C. 3 D. 4
1. 分别用浓度都为0.1mol/LNaCl的溶液、MgCl2溶液、AlCl3溶液与AgNO3溶液反应,产生质量相等的氯化银沉淀。消耗这三种溶液的体积比为 ( )
A . 1:2:3 B. 3:2:1 C. 2:3:6 D. 6:3:2
2.(03年江苏高考题)若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)( )
A 2ω1=ω2 B 2ω2=ω1 C ω2>2ω1 D ω1<ω2<2ω1
思维方法: 。
展望高考:
[巩固练习]
课堂反馈
 (1)溶液的稀释:
(1)溶液的稀释:
①V1p1×W1%= V2p2×W2% 或W液×W1%=(W液+W水)×W2%(溶质的质量守恒)
②C1V1=C2V2(溶质的物质的量守恒)
(2)溶液混合:C V=C2V2+C1V1(溶质的质量守恒)。
[例题解析]
[例1]某无水易溶盐X,摩尔质量为M g/mol,其溶解度为Sg.取其Wg加入VL
蒸馏水,配制成密度为d g/mL,质量百分浓度为A%,物质的量浓度为Cmol/L的澄
清溶液.下式表示正确的是
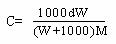
A.1000d×A%=C×M B.
C.S=100W/1000V D.A%=W/(W+1000V)%]
解题思路: 。
易错点: 。
[例2 ]已知98%的浓H2SO4的浓度为18.4mol· L-l,则49%的硫酸溶液的浓度为 ( )
A.等于9.2mol·L-1 B.大于9.2mol·L-1
C.小于9.2mol·L-1 D.不能确定
解题思路: 。
易错点: 。
[考题再现]
1.(03年江苏高考题)质量分数为a的某物质的溶液mg与质量分数为b的该物质的溶液ng混合后,蒸发掉pg水,得到的溶液每毫升质量为qg,物质的量浓度为c。则溶质的分子量(相对分子质量)为( )
A
 B
B 
C
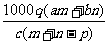 D
D 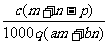
思维方法: 。
展望高考:
|
物理量 |
质量分数 |
物质的量浓度 |
溶解度 |
|
溶质单位 |
|
|
|
|
溶液单位 |
|
|
|
|
单 位 |
|
|
|
|
数值上关系 |
质量分数相同的两溶液其物质的量浓度一般 等. |
物质的量浓度相同的两溶液其质量分数一般 等. |
溶质溶解度相同的两溶液其在同一温度下饱和溶液的质量分数 等. |
|
定
义 |
|
|
|
|
符号 |
|
|
|
|
表达式 |
|
|
|
|
相同点 |
都能示溶质和溶液的相对比值 |
||
|
转化关系 |
|
2.c、 %、ρ之间的计算关系
%、ρ之间的计算关系

1.物质的量浓度的计算

2. 物质的量浓度溶液的配制
(1) 容量瓶
①特点:
②用途: 。容量瓶有各种不同规格,
常用的规格有100mL、250mL、500mL和1000mL等。
(2)配制一定体积物质的量浓度溶液的步骤及所用仪器如下:
(3)配制物质的量浓度溶液时,应注意的问题:
。
1.物质的量浓度
(1)概念:
(2)符号: (3)单位:
(4)说明:①物质的量浓度是溶液的体积浓度
②溶液中的溶质既可以为纯净物又可以为混合物,还可以是指某种
离子或分子。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com