
4、氧化钠与过氧化钠的比较
|
|
Na2O |
Na2O2 |
|
电子式 |
|
|
|
化学键键种类 |
|
|
|
nNa:nO |
|
|
|
n阳离子:n阴离子 |
|
|
|
类别 |
|
|
|
颜色状态 |
|
|
|
生成条件 |
|
|
|
与水反应 |
|
|
|
与盐酸反应 |
|
|
|
与CO2反应 |
|
|
3、钠的存在、保存、制法、用途
(1)少量金属钠可保存在 里,大量的金属钠则保存在 里
(2)钠的制法(化学方程式表示)
(3)钠的用途:
。
2.完成下列化学方程式
① Na + H2O →
解释实验现象; 浮 熔
游 红
② Na + H2O + FeCl3 →
③ Na + HCl →
④ C2H5OH + Na →
1.金属钠露置在空气中的变化过程(在下面括号中填写化学式)
银白色金属钠 → 表面变暗 → 出现白色固体 → 表面变成溶液
( ) ( ) ( ) ( )
→ 白色块状物质 → 白色粉末状物质
( ) ( )
金属钠质地 、 光泽,密度比水 ,能 于水,
熔点低。是 的良导体。
15.取一根镁条置于坩锅内点燃,得到氧化镁和氮化镁混合物的总质量为
470g. 冷却后加入足量水,将反应产物加热蒸干并灼烧,得到的氧化镁质
量为0.486g。
(1)写出氮化镁与水反应生成氢氧化镁和氨的化学方程式。
(2)计算燃烧所得混合物中氮化镁的质量分数。
14.为测定一种复合氧化物型的磁性粉末材料的组成,称取6.26g样品,将其全部溶于过量稀硝酸后,配成100mL溶液。取50mL溶液,加入过量K2SO4溶液,生成白色沉淀,经过滤、洗涤,烘干后得2.33g固体。另取25mL溶液,加入少许KSCN溶液,显红色。再取余下的25mL溶液,加入过量NaOH溶液,生成红褐色沉淀,将沉淀过滤、洗涤,灼烧后的0.80g固体。请计算并结合推理填写下表。
|
组成该磁性材料的元素是 |
|
|
各元素的质量比是 |
|
|
各元素的原子个数比是 |
|
|
该磁性材料的化学式为 |
|
13.A、B、C、D是四种可溶性离子化合物,其组成中的阴阳离子各不相同,它们在溶液中电离的阴、阳离子分别为Cl-、SO42-、NO32-、OH-、Ag+、Na+、Mg2+、Cu2+。当四种物质的稀溶液反应时产生如下现象①A + B → 产生白色沉淀;②B + D → 产生白色沉淀;③C + D → 产生蓝色沉淀。
由此可以判断(写分子式)A B C D 。
12.提示:某些金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空:
(1)单质F是
(2)写出由E生成G的离子反应方程式(或化学方程式)
(3)溶液I中所含金属离子是
(4)由C → E + F若改用浓酸,则不能选用的浓酸是(写分子式)

11.有一种工业废水,已知其中含有大量硫酸亚铁,少量Ag+和Na+。今设计一种既经济又合理的方法,回收银和硫酸亚铁。设计方案如下图所示,
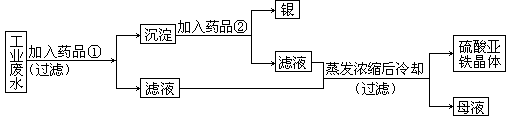
(1)药品①是
(2)沉淀是
(3)药品②是
(4)母液中存在的阳离子有
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com