
2.某酸溶液和某碱溶液恰好完全中和时,酸和碱液中一定相等的是( )
A.c(H+)和c(OH-) B.溶液的物质的量浓度
C.溶质的物质的量 D.所提供的H+和OH-的物质的量
1.下列几种情况对中和滴定结果无影响的是( )
A.盛待测液的锥形瓶里留有蒸馏水
B.滴定管尖嘴部分在滴定前有气泡,滴定后气泡消失
C.滴定管在滴定前未将刻度调在“0”,而调在“2.40”
D.滴定达终点时,俯视读数
2.(04年上海卷)氢氧化钡是一种使用广泛的化学试剂。某课外小组通过下列
实验测定试样中Ba(OH)2•nH2O的含量
(1) 称取3.50克试样溶于蒸馏水配成10ml溶液,从中取出10.0ml溶液于
锥形瓶中,加2滴指示剂,用0.100mol/L的HCl标准溶液滴定至终点,共
消耗标准液20.0ml(杂质不与酸反应)。求试样中氢氧化钡的物质的量。
(2) 另取5.25克试样加热至失去全部结晶水(杂质不分解),称得质量
为3.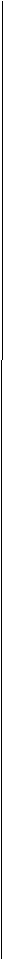 09克。求Ba(OH)2•nH2O中的n值。
09克。求Ba(OH)2•nH2O中的n值。
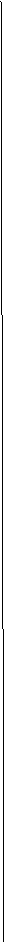 (3)试样中Ba(OH)2•nH2O的质量分数为
。
(3)试样中Ba(OH)2•nH2O的质量分数为
。
思维方法: 。
展望高考:
[巩固练习]
课堂反馈
1.(04年广东卷)甲酸和乙酸都是弱酸,当它们的浓度均为0.01mol•L-时,
甲酸中的c(H+)约为乙酸中的3倍。现有两种浓度不等的甲酸溶液a和b,
以及0.01mol•L-的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由
此可知: ( )
A. a的浓度必小于乙酸的浓度 B. a的浓度必大于乙酸的浓度
C. b的浓度必小于乙酸的浓度 D. b的浓度必大于乙酸的浓度
思维方法: 。
展望高考:
3.分析事例:在中和滴定操作过程中,对于以下各项因操作不当引起的实验误
差,用“偏高”“偏低”或“无影响”等填空:
(1)滴定管用蒸馏水洗净后,未用标准溶液润洗,使滴定结果_ _。
(2)锥形瓶用蒸馏水洗净后,又用待测溶液润洗,使滴定结果___ ______。
(3)标准液滴定管在滴定前尖嘴处有气泡,滴定终了无气泡,结果_______。
(4)滴定前平视,滴定终了俯视,使滴定结果___________。
(5)滴定前仰视,滴定终了平视,使滴定结果____________。
(6)过早估计终点,使滴定结果_______________。
(7)过晚估计终点,使滴定结果_______________,
(8)用含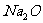 杂质的NaOH固体来配制已知浓度的标准溶液,用于滴定未知
杂质的NaOH固体来配制已知浓度的标准溶液,用于滴定未知
浓度的盐酸,使测得盐酸的浓度___________。
(9)用含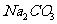 杂质的NaOH固体来配制已知浓度的标准溶液,用于滴定未
杂质的NaOH固体来配制已知浓度的标准溶液,用于滴定未
知浓度的盐酸,使测得盐酸的浓度___________。
(10)洗涤锥形瓶时,误把稀食盐水当做蒸馏水,然后用锥形瓶装待测的盐酸,
用NaOH标准溶液滴定时,对测得的结果______________。
[例题解析]
[例1] 用0.1mol/LNaOH溶液滴定100ml 0.1mol/L盐酸时,如果滴定误
差在±0.1%以内,反应完毕后,溶液的PH范围为( )
A.6.9-7.1 B.3.3-10.7 C.4.3-9.7 D.6-8
解题思路: 。
易错点: 。
[例2] 用中和滴定的方法测定NaOH和Na2CO3的混合溶液中NaOH的含量,可
先在混合液中加入过量的BaCl2溶液,使Na2CO3完全变成BaCO3沉淀,然后
用标准盐酸滴定(用酚酞作指示剂).试回答:
(1)滴定时BaCO3能否溶解?理由是
(2)如用甲基橙做指示剂,则测定的结果
解题思路: 。
易错点: 。
[考题再现]
2. 分析原理:据c标••••••V标••••n标=c待••V待•n待有n待=
。
分析原理:据c标••••••V标••••n标=c待••V待•n待有n待=
。
1. 产生误差的因素:(1)标准溶液不标准、(2)仪器洗涤未按要求、(3)滴定
管气泡未排尽、(4)滴定管读数方法不正确、(5)滴定管漏液、(6)终点判断
不准、(7)滴定操作过程和读数过快等
2.滴定:(1)用 移取一定体积的 到 中,加 ,
在瓶底垫 ;
(2)滴定时左手 、右手 、目光注视 。
(3)终点判断:① 、② 、
③ 、④ 。
(4)读数:注意: 。
(5)重复滴定:①目的 、
②当第二次读数与第一次读数误差很小时,是否需要进行第三次滴定
,当第二次读数与第一次读数误差较大时,应该
直到 为止,此时应该取 作为计算标准。
1.准备:(1) 、(2) 、
(3) 、(4) 、
(5) 、(6) 。
3.试剂:(1) 、 、 。
(2)指示剂的选择原则: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com