
1.2 质疑与对比
质疑:同一类的物质,化学性质是否相同?
对比:化学性质的差异表现及解释:①单质:S、O2、O3;②氢化物:H2S、H2O、H2O2。先引导示范(图5),然后分组讨论,最后交流总结。
交流:(唤起对感性表现的回忆,并进行分析,图6~8)








质疑:相同化合价的同种元素,其氧化性、还原性是否相同?
对比:根据物质的性质表现进行分析:①SO2、H2SO3、Na2SO3的还原性;②H2SO4(稀)与H2SO4(浓)氧化性。
交流:(在引导学生回忆具体物质氧化还原性的基础上,让学生分析物质性质的差异性,并从构成或结构角度进行分析[2],图9~10)




1.1 回顾与整理
提问:①氧族包括哪些元素?有规律地写出元素名称和符号。[氧O、硫S、硒Se、碲Te、钋Po]
②比较5种元素,为什么列为一族?[元素周期表第ⅥA族--位置,最外层电子数为6--结构]
③对比5种元素,选出代表元素并说明理由。
交流:(出现两组观点)
①O:“氧”作为这一族的名称;氧元素最为常见;氧元素在自然界中含量最高。
②S:ⅥA族中有3种固态非金属,硫最具代表性;硫元素的化合价较全面。
表决:(通过交流,学生的认识从感性走向理性)选择硫元素作为氧族元素的代表。
任务:按记忆规则写出常见含硫物质的化学式,并说明记忆的规则。
交流:(图1~3。注:图3中NaHSO3、NaHSO4因受图1中介绍的酸式盐影响而被另一学生补充)


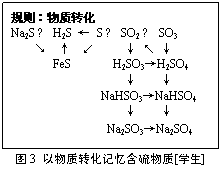
总结:以物质的组成分类、转化关系及S元素的化合价等方法记忆含硫物质有各自的优点。物质的组成结构决定物质的性质,因此物质的组成分类(属于组成和结构)决定化合价(属于化学性质)及转化关系(属于化学性质),兼顾考虑物质分类、化合价及转化关系等要素,可以设计更为全面的记忆图式。
整理:(通过交流,学生的视角从局部走向整体,图4)


18.机化学的记忆口诀
有机化学并不难,记准通式是关键。
只含C、H称为烃,结构成链或成环。
双键为烯叁键炔,单键相连便是烷。
脂肪族的排成链,芳香族的带苯环。
异构共用分子式,通式通用同系间。
烯烃加成烷取代,衍生物看官能团。
羧酸羟基连烃基,称作醇醛及羧酸。
羰基醚键和氨基,衍生物是酮醚胺。
苯带羟基称苯酚,萘是双苯相并联。
去H加O叫氧化,去O加H叫还原。
醇类氧化变酮醛,醛类氧化变羧酸。
羧酸都比碳酸强,碳酸强于石碳酸。
光照卤代在侧链,催化卤代在苯环。
烃的卤代衍生物,卤素能被羟基换。
消去一个小分子,生成稀和氢卤酸。
钾钠能换醇中氢,银镜反应可辨醛。
氢氧化铜多元醇,溶液混合呈绛蓝。
醇加羧酸生成酯,酯类水解变醇酸。
苯酚遇溴沉淀白,淀粉遇碘色变蓝。
氨基酸兼酸碱性,甲酸是酸又像醛。
聚合单体变链节,断裂π键相串联。
千变万化多趣味,无限风光任登攀。
17.酸和碱与指示剂反应
酸遇紫色石蕊变红,遇酚酞不变色,碱遇紫色石蕊变蓝,遇酚酞变红。
16.化学计算
化学式子要配平,必须纯量代方程, 单位上下要统一,左右倍数要相等。
质量单位若用克,标况气体对应升, 遇到两个已知量,应照不足来进行。
含量损失与产量,乘除多少应分清。
15.短周期元素化合价与原子序数的关系口诀
价奇序奇,价偶序偶。
14.化学反应基本类型口诀
化合多变一(A+B→C), 分解正相逆(A→B+C),
复分两交换(AB+CD→CB+AD),置换换单质(A+BC→AC+B)。
13.盐类溶解性表规律口诀
钾、钠铵盐都可溶,硝盐遇水影无踪;
硫(酸)盐不溶铅和钡,氯(化)物不溶银、亚汞。
12.盐类水解规律口诀
无“弱”不水解,谁“弱”谁水解;
愈“弱”愈水解,都“弱”双水解;
谁“强”显谁性,双“弱”由K定。
11.金属活动顺序表口诀
(初中)钾钙钠镁铝、锌铁锡铅氢、铜汞银铂金。
(高中)钾钙钠镁铝锰锌、铬铁镍、锡铅氢;铜汞银铂金。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com