
9.要鉴别己烯中是否混有少量甲苯,正确的实验方法是( )
A.先加足量的酸性高锰酸钾溶液,然后再加入溴水
B.先加足量溴水,然后再加入酸性高锰酸钾溶液
C.点燃这种液体,然后再观察火焰的颜色
D.加水,观察是否分层
8.下列除杂方法中正确的一组是( )
A.溴苯中混有溴,加入碘化钾溶液后用汽油萃取
B.乙醇中混有乙酸,加入NaOH溶液后用分液漏斗分液
C.乙烷中混有乙烯,通过盛有酸性KMnO4溶液的洗气瓶洗气
D.苯甲醛中混有苯甲酸,加入生石灰,再加热蒸馏
7.下列操作中错误的是( )
A.除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯
B.除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层
C.除去CO2中的少量SO2:通过盛有饱和NaHCO3溶液的洗气瓶
D.提取溶解在水中的少量碘:加入CCl4,振荡、静置分层后,取出有机层再分离
6.下列物质的分离、提纯和鉴别的方法中(必要时可加热),可行的是( )
A.以AgNO3溶液和稀盐酸检验溶液中是否含有Cl-
B.用升华法分离碘和氯化铵的混合物
C.以粗铜为阴极,精铜为阳极,CuSO4溶液为电解液,精炼铜
D.用NaOH溶液、蒸馏水和红色石蕊试纸检验溶液中是否含有NH4+
5.分离下列混合物,应选用蒸馏操作的是( )
A.汽油和柴油 B.溴水
C.硝酸钾和氯化钠的混合物 D.四氯化碳和水
4.下列各组物质中不易用物理性质区别的是( )
A.Na2CO3和CaCO3固体 B.酒精和汽油
C.氯化铵和硝酸铵晶体 D.碘和高锰酸钾固体
3.仅用蒸馏水,不能鉴别的一组物质是( )
A.苯和四氯化碳 B.溴蒸气和二氧化氮 C.碘和高锰酸钾 D.葡萄糖和蔗糖
2.鉴别苯酚、硫氰化钾、乙酸、氢氧化钠四种溶液,可用的一种试剂是( )
A.盐酸 B.食盐 C.新制的氢氧化铜 D.氯化铁
1.下列方法中,可用于除去小苏打溶液中混有的Na2CO3,最适宜的物质是( )
A.氢氧化钙 B. 通入CO2 C.碳酸氢钙 D.加入盐酸
2.阴离子的检验:
|
离子 |
检验试剂 |
实验现象 |
|
|
OH- |
①酚酞试液 ②石蕊试液 |
①呈红色 ②呈蓝色 |
|
|
Cl- |
AgNO3,稀HNO3 |
白色沉淀 |
Ag++Cl-=AgCl↓ |
|
Br- |
AgNO3,稀HNO3 |
淡黄色沉淀 |
Ag++Br-=AgBr↓ |
|
I- |
AgNO3,稀HNO3 |
黄色沉淀 |
Ag++I-=AgI↓ |
|
SO42- |
HCl,BaCl2溶液 |
加HCl无沉淀,再加BaCl2有白色沉淀 |
Ba2++SO42-=BaSO4↓ |
|
SO32- |
稀硫酸,品红溶液 |
无色有刺激性气味的气体,能使品红溶液退色 |
SO32-+2H+=SO2↑+H2O |
|
CO32- |
HCl,澄清石灰水 |
白色沉淀 |
CO32-+2H+=CO2↑+H2O CO2+Ca(OH)2=CaCO3+2H2O |
知识点3、常见物质的检验:
⑴ H2:灼热的CuO和CuSO4,黑色的CuO变红,白色CuSO4粉末变蓝色。
⑵ O2:带火星的木条,木条复燃。
⑶ CO:灼热的CuO和澄清石灰水,黑色的CuO变红,石灰水变浑浊。
⑷ CO2:气体通入石灰水,石灰水变浑浊。
⑸ Cl2:湿润的淀粉KI试纸,变蓝。
⑹ HCl:通入硝酸银和稀硝酸,产生白色沉淀。
⑺ SO2:品红溶液,品红溶液红色退去,再加热。又出现红色。
⑻ NH3:湿润的红色石蕊试纸,变蓝。
⑼ NO:打开瓶口与空气接触,立即变为红棕色气体。
知识点4、有机物的检验
⑴ 碳碳双键或三键:加少量溴水或酸性KMnO4溶液,褪色。
⑵ 甲苯:取两份甲苯,一份滴入溴水,振荡后上层呈橙色;另一份滴入酸性KMnO4溶液,振荡,紫色褪去。
⑶ 卤代烷:与NaOH溶液(或NaOH的醇溶液)共热后,先用硝酸酸化,再滴加AgNO3溶液,产生白色沉淀的为氯代烷,淡黄色沉淀的为溴代烷,黄色沉淀的为碘代烷。
⑷ 乙醇:将螺旋状铜丝加热至表面有黑色CuO生成,迅速插入待测溶液,反复多次,可见铜丝被还原成光亮的红色,并由刺激性气味产生。。
⑸ 苯酚:滴加过量的浓溴水,有白色沉淀;或滴加少量FeCl3溶液,溶液呈紫色。
⑹ 乙醛或葡萄糖:加入银氨溶液,水浴加热,产生银镜;或加入新制Cu(OH)2悬浊液加热至沸腾,有红色沉淀生成。
⑺ 乙酸:使石蕊试液变红;或加入Na2CO3或NaHCO3溶液有气泡;或加入新制Cu(OH)2悬浊液溶解得蓝色溶液。
⑻ 乙酸乙酯:加入滴加酚酞的NaOH溶液加热,红色变浅或消失。
⑼ 淀粉:滴加碘水,呈蓝色。
⑽ 蛋白质:灼烧,有烧焦羽毛气味;或加入浓硝酸微热,出现黄色。
知识点5、常见物质除杂方法
|
原物 |
所含杂质 |
除杂质试剂 |
主要操作方法 |
|
N2 |
O2 |
灼热的铜丝网 |
|
|
CO |
CO2 |
NaOH溶液 |
洗气 |
|
CO2 |
CO |
灼热CuO |
|
|
CO2 |
HCl |
饱和的NaHCO3 |
洗气 |
|
H2S |
HCl |
饱和的NaHS |
洗气 |
|
SO2 |
HCl |
饱和的NaHSO3 |
洗气 |
|
Cl2 |
HCl |
饱和的食盐水 |
洗气 |
|
CO2 |
SO2 |
饱和的NaHCO3或者酸性高锰酸钾溶液 |
洗气 |
|
炭粉 |
MnO2 |
浓盐酸(需加热) |
过滤 |
|
MnO2 |
C |
|
加热灼烧 |
|
炭粉 |
CuO |
稀酸(如稀盐酸) |
过滤 |
|
Al2O3 |
Fe2O3 |
NaOH(过量),CO2 |
过滤 |
|
Fe2O3 |
Al2O3 |
NaOH溶液 |
过滤 |
|
Al2O3 |
SiO2 |
盐酸、氨水 |
过滤 |
|
SiO2 |
ZnO |
HCl溶液 |
过滤 |
|
NaHCO3溶液 |
Na2CO3 |
CO2 |
加酸转化法 |
|
Na2CO3 |
NaHCO3 |
|
加热灼烧 |
|
FeCl3溶液 |
FeCl2 |
Cl2 |
加氧化剂转化法 |
|
FeCl2溶液 |
FeCl3 |
Fe |
加还原剂转化法 |
|
CuO |
Fe |
(磁铁) |
吸附 |
|
Fe(OH)3胶体 |
FeCl3 |
蒸馏水 |
渗析 |
|
I2晶体 |
NaCI |
|
加热升华 |
|
NaCl晶体 |
NH4Cl |
|
加热分解 |
|
KNO3晶体 |
NaCl |
蒸馏水 |
结晶. |
|
乙烯 |
SO2、H2O |
碱石灰 |
加固体转化法 |
|
乙烷 |
C2H4 |
溴的四氯化碳溶液 |
洗气 |
|
溴苯 |
Br2 |
NaOH稀溶液 |
分液 |
|
甲苯 |
苯酚 |
NaOH溶液 |
分液 |
|
己醛 |
乙酸 |
饱和Na2CO3 |
蒸馏 |
|
乙醇 |
水(少量) |
新制CaO |
蒸馏 |
|
苯酚 |
苯 |
NaOH溶液、CO2 |
分液 |
[典题分析]
例1.(2007年日照一轮考试题)现有三组混合液:①乙酸乙酯和乙酸钠溶液 ②乙醇和丁醇 ⑧溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
例2.(2006江苏高考化学试题)以下实验装置一般不用于分离物质的是( )
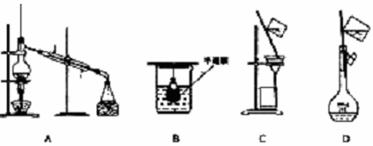
例3.(2006年全国高考四川卷)海带含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
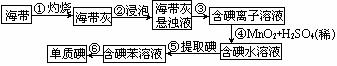
请填写下列空白:
(1)步骤①灼烧海带时,除需要三角架外,还需要用到的仪器是______________(从下列仪器中选择所需的仪器,用标号字母填写在空白处)
A、烧杯 B、坩埚 C、表面皿 D、泥三角 E、酒精灯 F、干燥器
(2)步骤③的实验操作名称是_______________;步骤⑥的目的是从含碘苯溶液中分离出碘和回收苯,该步骤的实验操作名称是_____________________。
(3)步骤④反应的离子方程式是____________________________________________________。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是____________________________________。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法___________________
_________________________________________________________________________________。
例4.(2006年高考化学预测题)现有一种含有Ag+、Al3+、Mg2+、Ba2+的混合溶液,如果要通过依次加入四种离子,使上述四种金属离子依次成为沉淀从溶液中分离出来,则加入的四种离子是什么,顺序如何?试写出两种可能的情况。
__________________________________________________________________________________
__________________________________________________________________________________
__________________________________________________________________________________
例5.(2006年高考化学预测题)在一含Na+的澄清溶液中,可能还存在NH4+、Fe2+、I-、Br-、CO32-、SO32-六种离子中的几种。①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③橙黄色溶液不能使淀粉溶液变蓝色。根据上述实验事实推断,下列说法不正确的是 ( )
A.溶液中一定存在Br-、CO32- B.溶液中可能存在NH4+
C.溶液中一定不存在Fe2+、I-、SO32- D.溶液一定呈碱性
例6.(2006年南京市高三质量检测题)一定量某有机物溶解于适量的NaOH溶液中,滴入酚酞,溶液呈红色,煮沸5min后,溶液颜色变浅,再加入盐酸显酸性,沉淀出白色晶体。取少量晶体放到FeCl3溶液中,溶液呈紫色,则该有机物可能是( )

例7.(2007年日照市模拟试题)只用一种试剂,区别甲苯、四氯化碳、己烯、乙醇、碘化钾溶液、亚硫酸六种无色液体,应选用( )
A.酸性KMnO4溶液 B.溴水 C.碘水 D.硝酸银溶液
例8.(2007年潍坊市模拟试题)下列各组物质,只用水不能鉴别的是( )
A.白色粉末:CuSO4、Na2CO3、CaCO3 B.无色液体:乙醇、苯、四氯化碳
C.白色粉末:NaOH、NaCl、NH4NO3 D.无色液体:苯、甲苯、乙醛
[演练提高]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com